Những nội dung chính
Được phát minh nằm 1927, nhưng chỉ sau hơn 2 thập kỷ, dao điện đã trở nên phổ biến trên khắp thế giới. Sự ra đời của dao điện đã thay đổi đáng kể bộ mặt của phẫu thuật với những lợi ích mà nó mang lại, như cắt nhanh, cầm máu hiệu quả, sử dụng dễ dàng, an toàn và hiệu quả kinh tế. Kết quả tất yếu là ngày nay dao điện trở thành một phương tiện không thể thiếu trong hầu hết các phòng mổ.
Tuy nhiên, dao điện có thực sự an toàn như những gì chúng ta vẫn nghĩ?

Nguyên lý hoạt động của dao điện là tạo ra nhiệt, nhờ dòng điện đi qua mô, để thực hiện phân tách và cầm máu. Nhiệt độ cao nhất của dao là 214,4oC ở 20W; 301,7oC ở 60W; 436,6oC ở 70W và 500oC ở 80W. Trong quá trình sử dụng dao điện, nhiệt độ cao của đầu dao đã nhiệt phân tổ chức mô và giải phóng một lượng khói đáng kể, được gọi là “khói phẫu thuật” (surgical smoke).
Khói phẫu thuật được mô tả như “canh hóa chất” (chemical soup), thứ mà hiện diện ở bất cứ nơi nào có phẫu thuật và thủ thuật xâm lấn. Các thành phần của “canh hóa chất” này bao gồm 95% nước và 5% các thành phần sau:
- Khí độc
- Hơi và các hạt
- Tế bào sống và chết
- Virus và vi khuẩn.
Với sự tiến bộ của khoa học – kỹ thuật, càng nhiều trang thiết bị y tế hiện đại được đưa vào sử dụng trong quá trình phẫu thuật. Một trong số đó là dao siêu âm và dao laser. Những thiết bị này cùng với dao điện để tạo nên “canh hóa chất” trong phòng mổ hiện đại.
Mặc dù phòng mổ được xem là môi trường sạch sẽ nhất trong các cơ sở y tế, do những yêu cầu vô trùng của phẫu thuật, nhưng khói phẫu thuật có thể ảnh hưởng đến sức khỏe của những người có mặt trong phòng mổ, bao gồm cả nhân viên y tế và bệnh nhân. Ngoài chứa mùi khó chịu, khói phẫu thuật còn chứa những chất gây ung thư, ảnh hưởng đến hàng triệu nhân viên phòng mổ (operating room personnel) trên toàn thế giới [1].
1. Hóa chất trong khói phẫu thuật
Trong phòng mổ, khói phẫu thuật chứa nhiều khí và các thành phần hóa học với kích thước khác nhau, có liên quan đến các nguy cơ sức khỏe của nhân viên phòng mổ. Trong khói phẫu thuật có chứa hydrocarbon, phenol, nitriles, acid béo, acrolonitril carbon monoxid và các vi sinh vật có thể gây ra các vấn đề sức khỏe [2],[3],[4]. Có đến 8 loại hóa chất là những tác nhân gây ung thư được tìm thấy trong khói phẫu thuật.
Các hóa chất giải phóng ra từ 1g mô bị đốt bởi dao điện tương đương với 6 điếu thuốc [5]. Hill và cộng sự ghi nhận, khói được tạo ra trong phòng mổ mỗi ngày tương đương với 27 – 30 điếu thuốc lá [6].
Mô da sẽ tạo ra nồng độ các hóa chất và các hạt cao hơn so với mô mỡ và mô cơ. Do vậy, nên sử dụng dao lạnh để cắt da và sử dụng chế độ cầm máu của dao điện để cầm những vị trí chảy máu, sẽ giúp giảm nồng độ chất gây ung thư trong khói phẫu thuật. Nên hạn chế sử dụng chế độ cầm máu với mô mỡ và mô bạch huyết [7].
1.1. Polycyclic aromatic hydrocarbons, benzo[a]pyren: Những tác nhân gây ung thư
Tác nhân gây ung thư chính trong khói phẫu thuật là polycyclic aromatic hydrocarbons (PAHs), ngoài ra benzo[a]pyren (BaP) cũng được chứng minh có thể gây ra ung thư [8],[9],[10],[11]. PAHs có thể hoạt hóa các receptor estrogen, tác động trực tiếp hoặc gián tiếp vào quá trình tổng hợp estrogen. PAHs kích thích sự nhân lên của các tế bào ung thư vú phụ thuộc vào estrogen. BaP là một tác nhân gây đột biến mạnh, làm giảm sự biểu hiện của gen ức chế ung thư p53 do vậy kích thích sự hình thành các tế bào ung thư.
Khói phẫu thuật, cùng với PAHs, đi vào phổi trong quá trình hít thở, gây ra những đe dọa tiềm tàng về hô hấp. Cơ quan bảo vệ môi trường Hoa Kỳ đã liệt kê đến 16 loại PAHs có độc tính và nguy cơ gây ung thư [7]. Một phân tích gộp của Cơ quan nghiên cứu ung thư quốc tế (international Agency for Research on Cancer – IARC) cho thấy ung thư phổi là ung thư phổ biến nhất liên quan với PAH.

Để đánh giá nồng độ các hóa chất trong khói phẫu thuật, Tseng và cộng sự đã tiến hành một nghiên cứu với những bệnh nhân được phẫu thuật cắt toàn bộ tuyến vú, ở hai bệnh viện khác nhau [13]. Nhóm nghiên cứu lựa chọn những ca phẫu thuật cắt toàn bộ tuyến vú vì thời gian phẫu thuật kéo dài và dao điện được sử dụng đáng kể. Trước phẫu thuật, phòng mổ được vệ sinh sạch sẽ và được làm sạch đến mức 104 (tức số hạt có kích thước lớn hơn 0,5µm dưới 104/ft3 – mỗi ft3 tương đương với 0,0283m3 hoặc 28,3 lít). Mẫu khí trước phẫu thuật được thu thập để so sánh.
Trong quá trình phẫu thuật, dao điện được duy trì ở mức 25W trở xuống. 14 ca phẫu thuật cắt toàn bộ tuyến vú được thu thập mẫu khí/hạt trong không khí. Trong suốt quá trình phẫu thuật, nồng độ các hạt có kích thước 0,3; 0,5; 1; 3; 5; 10 µm được theo dõi cẩn thận bằng máy đếm laser, cứ mỗi 5 phút, cho đến khi kết thúc phẫu thuật.
Để đánh giá mức độ phơi nhiễm của nhân viên phòng mổ, các mẫu không khí được lấy cách trường mổ 30cm, tương ứng với khoảng không gian mà phẫu thuật viên (surgeon) và gây mê (anesthetic technologist – AT) hít thở. Các mẫu khí và hạt trong không khí được thu thập với tốc độ 30L/phút. Sau đó không khí này được dẫn qua các sợi lọc thạch anh 47mm để thu gom khói và giữ lại các khí gây ô nhiễm bằng bọt polyurethane. PAHs được thu thập qua nhiều công đoạn với hiệu quả trung bình 85% (từ 52% đến 114%).
Tất cả các bệnh nhân trong nghiên cứu đều được thông báo và nhận được sự đồng ý.
Kết quả nghiên cứu:
– Thời gian sử dụng dao điện chiếm 1/3 thời gian phẫu thuật. Việc sử dụng dao điện liên tục đã tạo nên một lượng đáng kể khói và các hạt không nhìn thấy trong không khí.
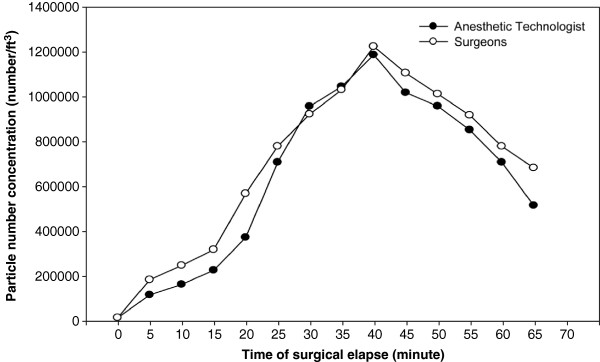
– Phần lớn các hạt có kích thước 0,3µm, chiếm 70% số hạt. Đường kính các hạt trong không khí trung bình là 0,35µm (95% CI: 0,32-0,38µm).
– Nồng độ các hạt cao nhất là 1,2 x 106/ft3, được tìm thấy ở khu vực thở của phẫu thuật viên (phía dưới đèn phẫu thuật), sau đó là khu vực gây mê.
– Nồng độ PAHs tại vị trí của phẫu thuật viên và gây mê tăng gấp 40-100 lần so với nồng độ PAHs trước phẫu thuật. Phẫu thuật viên tiếp xúc với PAHs gấp 1,5 lần so với gây mê do khoảng cách với trường mổ của phẫu thuật viên là gần nhất. Nồng độ PAHs trong khói gấp 30 lần trong hạt.
– Nguy cơ ung thư mà PAHs gây ra cho phẫu thuật viên và gây mê lần lượt là 46,8×10-6 và 29,3×10-6, với mỗi giờ tiếp xúc. Dù nguy cơ mỗi giờ của gây mê chỉ bằng 62% so với phẫu thuật viên, nhưng thời gian làm việc trong phòng mổ kéo dài, nên nguy cơ của gây mê tăng lên đáng kể. Nguy cơ ung thư trong 70 năm cuộc đời của phẫu thuật viên và gây mê lần lượt là 117×10-6 và 270×10-6, cao hơn đáng kể so với khuyến cáo an toàn của WHO là 1×10-6.
1.2. Carbon monoxid
Một trong số các thành phần hóa học của khói phẫu thuật là carbon monoxid (CO), tác nhân có thể gây nguy hiểm cho sức khỏe của tất cả các nhân viên y tế trong phòng mổ. Chỉ sau 5 phút sử dụng dao điện trong phẫu thuật nội soi ổ bụng, CO đã xuất hiện trong ổ bụng của bệnh nhân với nồng độ trung bình là 345 ppm (25-1600ppm) và khi kết thúc cuộc mổ là 475pp (100-1900ppm). Cao hơn rất nhiều so với với giới hạn 35ppm cho mỗi giờ tiếp xúc của Cơ quan bảo vệ môi trường (Environmental Protection Agency) [1].
1.3. Các hạt PM2.5
Nguy cơ sức khỏe của khói phẫu thuật còn được gây ra bởi những hạt có đường kính dưới 2,5µm (PM2.5), vì những kích thước nhỏ của những hạt này đi vào các phế nang và hệ thống tuần hoàn, gây ra những vấn đề cho não, gan, tim và thận. Các mô có thể tạo ra các hạt PM2.5 với nồng độ trên 150 µg/m3. Đây là giới hạn không tốt cho sức khỏe theo tiêu chuẩn của Liên minh châu Âu [13].
2. Vi sinh vật
Ngoài các chất hóa học, khói phẫu thuật còn chứa các sản phẩm sinh học. HPV được tìm thấy trong khói của dao điện và dao laser trong quá trình điều trị u nhú thanh quản (laryngeal papilloma) [14] và nhiễm trùng sinh dục (genital infection) [15]. Gloster và cộng sự tìm thấy HPV trong mũi họng của phẫu thuật viên laser [16]. Những nghiên cứu gần đây khẳng định phẫu thuật viên có nguy cơ phơi nhiễm HPV do khói của dao điện và dao laser [17].
Khói phẫu thuật còn chứa virus viêm gan B (HBV). Kwak đã thực hiện nghiên cứu trên 11 bệnh nhân được phẫu thuật nội soi ổ bụng và phẫu thuật robot ổ bụng. Tất cả bệnh nhân có kháng nguyên bề mặt viêm gan B (HBsAg) dương tính. Tải lượng virus trong máu của bệnh nhân từ khoảng không phát hiện được đến 1,7×108 IU/ml. Kết quả: HBV được tìm thấy trong khói phẫu thuật của 10 trong số 11 bệnh nhân [18].
Ngoài HPV và HBV, DNA của virus HIV, vi khuẩn Staphylococcus và Neisseria cũng được tìm thấy trong khói phẫu thuật [5].
3. Các biện pháp phòng tránh
Mặc dù khói phẫu thuật đã được nhiều nghiên cứu chứng minh nguy cơ đối với sức khỏe của nhân viên phòng mổ, nhưng có một tỷ lệ đáng kể nhân viên phòng mổ chưa từng biết về những nguy cơ đó. Theo kết quả khảo sát của Viện Quốc gia về An toàn và Sức khỏe Nghề nghiệp (NIOSH), tại Hoa Kỳ có đến 49% người sử dụng dao laser và 44% người sử dụng dao điện trong phẫu thuật được hỏi trả lời rằng họ chưa bao giờ được đào tạo về nguy cơ của khói phẫu thuật với sức khỏe. Có đến 98% người sử dụng dao điện chỉ dùng khẩu trang phẫu thuật, cái mà không thể bảo vệ hoàn toàn đường hô hấp.
– Khẩu trang
Có sự khác biệt lớn về hiệu quả lọc của các loại khẩu trang, từ 13% đến 99% [19]. Khẩu trang phẫu thuật không thể bảo vệ khỏi khói phẫu thuật, do không kín hoàn toàn và không có hiệu quả lọc những hạt kích thước nhỏ. Chỉ có khẩu trang N95 có hiệu quả hơn thiết bị hút khói trong quá trình phẫu thuật.

– Đảm bảo thông khí: Sử dụng hệ thống hút khói, đặc biệt là bộ lọc không khí hiệu quả cao (High Efficiency Particulate Air filters).
Tóm lại, phòng mổ được xem là nơi sạch sẽ nhất của các bệnh viện, nhưng môi trường trong phòng mổ không “sạch” như chúng ta vẫn nghĩ. Khói phẫu thuật được tạo ra từ dao điện, dao siêu âm, dao laser, có chứa nhiều hóa chất độc hại, cũng như vi khuẩn và virus (HPV, HIV, HBV). PAHs, là chất đã được chứng minh có thể gây ung thư, hiện diện với nồng độ đáng kể trong khói phẫu thuật. Nguy cơ ung thư của nhân viên phòng mổ cao gấp 117-270 lần so với khuyến cáo an toàn của WHO. Để giảm việc tiếp xúc với các hạt và khói trong phẫu thuật, nên kết hợp khẩu trang N95 và thiết bị hút khói, đặc biệt là bộ lọc không khí hiệu quả cao.
BS. Lê Văn Thành – Bệnh viện K
TÀI LIỆU THAM KHẢO
1. Beebe D.S., Swica H., Carlson N., et al. (1993). High Levels of Carbon Monoxide Are Produced by Electro-Cautery of Tissue During Laparoscopic Cholecystectomy:. Anesthesia & Analgesia, 77(2), 338–341.
2. Barrett W.L. and Garber S.M. (2003). Surgical smoke: a review of the literature. Surgical Endoscopy, 17(6), 979–987.
3. Hensman C., Baty D., Willis R.G., et al. (1998). Chemical composition of smoke produced by high-frequency electrosurgery in a closed gaseous environment: An in vitro study. Surg Endosc, 12(8), 1017–1019.
4. Garden J.M. (1988). Papillomavirus in the Vapor of Carbon Dioxide Laser-Treated Verrucae. JAMA, 259(8), 1199.
5. Addley S. and Quinn D. (2018). 1408 Surgical smoke – what is it and what are the risks? a review. Occupational Health for Health Care Workers, BMJ Publishing Group Ltd, A321.1-A321, A321.1-A321.
6. Hill D.S., O’Neill J.K., Powell R.J., et al. (2012). Surgical smoke – a health hazard in the operating theatre: a study to quantify exposure and a survey of the use of smoke extractor systems in UK plastic surgery units. J Plast Reconstr Aesthet Surg, 65(7), 911–916.
7. Cheng P.-C., Wen M.-H., Hsu W.-L., et al. (2021). A study to quantify surgical plume and survey the efficiency of different local exhaust ventilations. Sci Rep, 11(1), 14096.
8. Menzie C.A., Potocki B.B., and Santodonato J. (1992). Exposure to carcinogenic PAHs in the environment. Environ Sci Technol, 26(7), 1278–1284.
9. Tang D., Cho S., Rundle A., et al. (2002). Polymorphisms in the DNA Repair Enzyme XPD are Associated with Increased Levels of PAH–DNA Adducts in a Case-Control Study of Breast Cancer. Breast Cancer Res Treat, 75(2), 159–166.
10. Yan J., Wang L., Fu P.P., et al. (2004). Photomutagenicity of 16 polycyclic aromatic hydrocarbons from the US EPA priority pollutant list. Mutation Research/Genetic Toxicology and Environmental Mutagenesis, 557(1), 99–108.
11. Plísková M., Vondrácek J., Vojtesek B., et al. (2005). Deregulation of cell proliferation by polycyclic aromatic hydrocarbons in human breast carcinoma MCF-7 cells reflects both genotoxic and nongenotoxic events. Toxicol Sci, 83(2), 246–256.
12. Tseng H.-S., Liu S.-P., Uang S.-N., et al. (2014). Cancer risk of incremental exposure to polycyclic aromatic hydrocarbons in electrocautery smoke for mastectomy personnel. World J Surg Onc, 12(1), 31.
13. Karjalainen M., Kontunen A., Saari S., et al. (2018). The characterization of surgical smoke from various tissues and its implications for occupational safety. PLoS ONE, 13(4), e0195274.
14. Kashima H.K., Kessis T., Mounts P., et al. (1991). Polymerase Chain Reaction Identification of Human Papillomavirus DNA in CO2 Laser Plume from Recurrent Respiratory Papillomatosis. Otolaryngol Head Neck Surg, 104(2), 191–195.
15. Zhou Q., Hu X., Zhou J., et al. (2019). Human papillomavirus DNA in surgical smoke during cervical loop electrosurgical excision procedures and its impact on the surgeon. CMAR, Volume 11, 3643–3654.
16. Gloster H.M. and Roenigk R.K. (1995). Risk of acquiring human papillomavirus from the plume produced by the carbon dioxide laser in the treatment of warts. Journal of the American Academy of Dermatology, 32(3), 436–441.
17. Bigony L. (2007). Risks Associated with Exposure to Surgical Smoke Plume: A Review of the Literature. AORN Journal, 86(6), 1013–1024.
18. Kwak H.D., Kim S.-H., Seo Y.S., et al. (2016). Detecting hepatitis B virus in surgical smoke emitted during laparoscopic surgery. Occup Environ Med, 73(12), 857–863.
19. Redmayne, A.C., D. Wake, R. C. Brown, et al. (1997). Measurement of the Degree of Protection Afforded by Respiratory Protective Equipment Against Microbiological Aerosols. The Annals of Occupational Hygiene, 41(inhaled_particles_VIII), 636–640.
 UNG THƯ HỌC
UNG THƯ HỌC



