Những nội dung chính
Đặt vấn đề
Khối tân sản thần kinh nội tiết (Neuroendocrine neoplasms – NENs) là những tổ chức tân sản có nguồn gốc từ hệ thống tế bào thần kinh nội tiết, có thể lành tính hoặc ác tính [1]. Mặc dù chúng có thể phát triển ở hầu hết mọi cơ quan, NEN bắt gặp nhiều hơn ở tuyến tụy và hệ tiêu hóa (Gastroenteropancreatic (GEP)-NENs), nơi chúng được cho là bắt nguồn từ các tiểu đảo Langerhans và các tế bào Enterochromaffin của ống tiêu hóa [2]. GEP – NENs là loại ung thư tiêu hóa đứng thứ hai theo mức độ phổ biến. Ở Hoa Kỳ, tỷ lệ mắc hàng năm dao động từ 2 đến 5 trên 100.000 bệnh nhân, và sự gia tăng ổn định tần suất đã được ghi nhận trong ba thập kỷ qua [3].
Cũng như các loại ung thư thư khác, di căn xa (Metastatic NENs – mNENs) là môt trong những yếu tố hàng đầu ảnh hưởng đến tiên lượng sống của bệnh nhân. Trong khi, phân tích dựa trên cơ sở dữ liệu SEER cho thấy thời gian sống thêm trung vị toàn bộ (median overall survival – OS) của GEP-NENs là 9.3 năm ở Hoa Kỳ [4], các nghiên cứu dựa trên dân số báo cáo rằng thời gian OS cho những bệnh nhân có mNENs tụy và ruột non tương ứng chỉ đạt 24 và 56 tháng [5]. Điều này đặt ra yêu cầu phối hợp nhiều phương pháp điều trị nhằm nâng cao kỳ vọng sống dành cho những trường hợp này.
Việc điều trị GEP-NENs đòi hỏi một cách tiếp cận đa chuyên khoa. Trong khi phẫu thuật cắt bỏ tiếp theo là giám sát tích cực vẫn là nền tảng chính để điều trị NENs khu trú, việc điều trị bệnh nhân mNENs cần đến sự kết hợp của các phương pháp tiếp cận toàn thân và khu vực khác. Bài viết này xin tóm tắt những tiến bộ gần đây trong điều trị GEP-NENs tiến triển, mô tả các phương pháp tiếp cận có thể để điều trị nhóm bệnh ác tính này.
Các phương pháp điều trị
Các liệu pháp sinh học (Biological therapies)
Đồng phân Somatostatin (Somatostatin Analogues)
Bên cạnh vai trò ngăn cản sự bài tiết của các hoạt chất sinh học, SSA là thuốc điều trị đầu tay nhằm kìm hãm sự phát triển của khối u. Thử nghiệm PROMID cho thấy Octreotide giải phóng chậm (Octreotide LAR) liều 30 mg tiêm bắp 1 tháng 1 lần có tác dụng kìm hãm sự phát triển của khối u trên những bệnh nhân u thần kinh nội tiết đoạn ruột giữa thế G1 biệt hóa cao đã di căn. Thời gian sống thêm không bệnh trung vị trên nhớm có dùng Octreotide LAR so với nhóm giả dược là 14.3 tháng so với 6 tháng (p=0.000072) [6]. Tuy nhiên nghiên cứu gần đây của Rinke A. và cộng sự cho thấy không có sự khác biệt về lợi ích sống thêm dài hạn trên bệnh nhân sử dụng Octreotide LAR so với nhớm giả dược [7]. Thử nghiệm lâm sàng CLARINET so sánh Lancreotide dạng hỗn dịch giải phóng chậm với liều 120 mg so với giả dược trên bệnh nhân giai đoạn tiến triển, không chức năng, thụ thể Somatostatin dương tính typ G1 và G2 (Ki-67<10%) u thần kinh nội tiết tụy-ống tiêu hóa, kết quả cho thấy Lancreotide cho thời gian sống thêm không bệnh trung vị cao hơn có ý nghĩa [8].
Interferon (IFN) alpha
Interferon-α hay INF-α được coi là phương pháp điều trị cuối cùng dành cho những trường hợp bệnh giai đoạn muộn, tiến triển [9]. Một thử nghiệm lâm sàng đối chứng ngẫu nhiên trên 65 bệnh nhân u thần kinh nội tiết đoạn ruột giữa đã được phẫu thuật hoặc nút hóa chất động mạch gan cho thấy không có sự khác biệt về sống còn giữa 2 nhóm điều trị bằng Octreotide đơn thuần so với nhóm kết hợp Octreotide với INF-α. Mặc dù vậy, INF-α làm giảm đáng kể nguy cơ tiến triển của khối u (HR: 0.28; Độ tin cậy 95% [95% CI]: 0.16-0.45) [10]. Một thử nghiệm lâm sàng pha III được thực hiện bới Nhóm Ung thư học Tây Bắc (Southwest Oncology Group – SWOG) trên nhóm bệnh nhân u Carcinoid tiến triển cho thấy không có sự khác biệt về thời gian sống thêm không bệnh giữa nhóm sử dụng bevacizumab và nhóm sử dụng INF-α (2 nhóm cùng được sử dụng Octreotide kèm theo), tuy nhiên thời gian cho tới khi điều trị thất bại cao hơn đáng kể ở nhóm bevacizumab so với nhóm interferon [11]. Biến chứng hay gặp của INF-α bao gồm mệt mỏi và hội chứng giả cúm. Pegylated interferon (PEG-IFN) được cho là có thể giảm bớt các biến chứng nêu trên [12]. Tuy vậy, có thể thấy, việc không mang lại lợi ích lớn cũng như có nhiều tác dụng phụ đã làm hạn chế việc sử dụng INF-α trên lâm sàng [1].
Telotristat ethyl
Telotristat ethyl (Xermelo) là một chất ức chế enzyme oxy hóa khử Trytophan, một enzyme đóng vai trò trong quá trình tổng hợp các SSA hệ tiêu hóa. Chất này có thể dùng cho những trường hợp tiêu chảy đề kháng với SSA trong hội chứng Carcinoid. Thử nghiệm pha 3 TELESTAR và nghiên cứu TELECAST có sự liên quan có ý nghĩa giữa lượng 5-HIAA nước tiểu với tình trạng nhu động ruột trong ngày. Tăng các enzyme transaminases và triệu chứng buồn nôn cũng được quan sát thấy trong những nghiên cứu này [13], [14].
Các phương pháp điều trị đích (Targeted therapies)
Chất ức chế thụ thể rapamycin trên động vật có vú (Mammalian (mechanistic) Target of Rapamycin (mTOR) inhibitors)
Everolimus là chất ức chế thụ thể rapamycin trên động vật có vú (the mammalian target of rapamycin – mTOR), một yếu tố kích thích trong chu kỳ tế bào và chuyển hóa. Thử nghiệm lâm sàng RADIANT-4 cho thấy everolimus làm tăng có ý nghĩa thời gian sống thêm không bệnh trên nhóm u thần kinh nội tiết giai đoạn tiến triển, không chức năng, biệt hóa cao của phổi và hệ tiêu hóa (11 so với 3.9 tháng, p<0.00001) [15]. Mặc dù everolimus có một số nguy cơ gây nên những tác dụng phụ nguy hiểm, chất lượng cuộc sống là hoàn toàn chấp nhận được so với nhóm giả dược, hơn nữa, hoạt tính của everolimus không bị ảnh hưởng bởi việc sử dụng các loại thuốc SSA trước đó [16], [17].
Chất ức chế enzyme Tyrosine Kinase (Tyrosine Kinase Inhibitors – TKI)
Sunitinib là một TKI (tyrosine kinase inhibitor) có vai trò ức chế các chất tạo mạch thường xuất hiện trong nhóm u thần kinh nội tiết có tăng sinh mạch. Với u thần kinh nội tiết tuyến tụy biệt hóa cao giai đoạn tiến triển, Sunitinib làm tăng thời gian sống thêm không bệnh so với nhóm giả dược (11 so với 5 tháng, p<0.001) [18], [19]. Tuy nhiên giá thành của phương pháp điều trị này vẫn là một vấn đề lớn.
Liệu pháp sử dụng phân tử Peptide gắn đồng vụ phóng xạ (Peptide receptor radionuclide therapy – PRRT)
Liệu pháp này sử dụng các đồng phân SSA làm các phân tử mang đồng vị phóng xạ phân ra tia ß. Các đồng phân SSA gắn đồng vị phóng xạ sẽ gắn vào các receptor đặc hiệu trên bề mặt các tế bào u thần kinh nội tiết, từ đó từ đó giải phóng ra các tia phóng xạ tiêu diệt tế bào ung thư [20]. Như vậy, kết quả đáp ứng phụ thuộc vào mức độ biểu hiện của receptor Somastatin trên bề mặt tế bào ung thư. Một số hợp chất SSA có gắn đồng vị phóng xạ đã và đang được nghiên cứu , bao gồm ¹¹¹In-DTPA, ⁹⁰Y-DOTATOC và ¹⁷⁷Lu-DOTATATE [21]. Thử nghiệm lâm sàng NET-TER-1 cho thấy với bệnh nhân u thần kinh nội tiết ruột giữa giai đoạn muộn, tiến triển, thụ thể SSA dương tính thì ¹⁷⁷Lu-DOTATATE với phác đồ octreotide phân giải chậm làm tăng thời gian sống thêm không bệnh so với việc tăng liều octreotide giải phóng chậm đơn thuần, với thời điểm nghiên cứu cut-off ở 20 tháng (65.2% so với 10.8%). Tuy nhiên, các tác dụng phụ như giảm bạch cầu, giảm tiểu cầu, giảm bach cầu lympho được quan sát thấy ở nhóm sử dụng ¹⁷⁷Lu-DOTATATE [22].
Hóa trị thông thường
U thần kinh nội tiết giai đoạn tiến triển (xấm lấn khu vực và di căn) thường không còn khả năng điều trị khỏi, các thuốc gây độc tế bào có thể sử dụng để kiểm soát bệnh tùy theo phân loại mô bệnh học của khối u. Các thuốc có thể sử dụng bao gồm nhóm Alkyl (streptozocin, dacarbazine và temozolomide), nhóm ức chế chuyển hóa tế bào (5-fluorouracil và capecitabine) và nhóm anthracycline (doxorubicin và epirubicin). Nhiều thử nghiệm lấm sàng pha II và III nhằm đánh giá hiệu quả của việc sử dụng đơn độc cũng như kết hợp các nhóm thuốc nêu trên. Các nghiên cứu cũ hướng tới đánh giả hiệu quả của việc sử dụng streptozocin đơn độc với việc kết hợp với 5-fluorouracil hoặc doxorubicin, kết quả cho thấy việc sử dụng phối hợp làm tăng đáng kể tỷ lệ đáp ứng và thời gian sống thêm trung vị [23]. Một nghiên cứu pha II/III gần đây của Sun W. và cộng sự so sánh kết quả điều trị giữa phác đồ 5-fluorouracil kết hợp với doxycycline hoặc streptozocin, kết quả cho thấy phác đồ 5-fluorouracil kết hợp với streptozocin làm tăng thời gian sống thêm so với phác đồ còn lại [24]. Thêm vào đó, một thử nghiệm lâm sàng pha II so sánh giữa capecitabine đường uống, một tiền chất của 5-fluorouracil so với 5-fluorouracil đường tĩnh mạch, cho thấy kết quả điều trị tương tự nhưng tác dụng phụ ít hơn đáng kể (chủ yếu là tiêu chảy và mệt mỏi) [25]. Irinotecan/cisplatin (IP) và etoposide/cisplatin (EP) là những phác đồ hóa chất thông dụng nhất đối với ung thư thần kinh nội tiết giai đoạn tiến triển [26]. Một số nghiên cứu cho thấy capecitabine kết hợp với temozolomide (CAPTEM) [27], bevacizumab [28], hay 5-fluorouracil [29] và streptozotocin [30] hoàn toàn có thể áp dụng với những trường hợp u thần kinh nội tiết đường tiêu hóa không còn khả năng cắt bỏ. Mặc dù vậy, với mức độ bằng chứng trên, việc sử dụng hóa chất vẫn còn nhiều tranh cãi, chủ yếu do những độc tính của các phác đồ này gây ra nếu được sử dụng rộng rãi. Tuy nhiên, đây vẫn là những lựa chọn đáng cân nhắc cho những bệnh nhân phù hợp [31].
Điều trị miễn dịch (Immunotherapy)
Liệu pháp miễn dịch là một lĩnh vực điều trị phát triển nhanh chóng trong các loại ung thư khác nhau. Các con đường miễn dịch hoạt động một cách sinh lý để ngăn chặn các tế bào T được kích hoạt theo một cơ chế tự miễn. Thụ thể chết theo lập trình 1 (Programmed death receptor 1 or PD-1) là một thụ thể ức chế nằm trên tế bào T tương tác với các phối tử PD-L1 và PD-L2 của nó để làm giảm phản ứng kháng u của tế bào T. Trong nghiên cứu sơ bộ, người ta đã chỉ ra rằng các kháng thể chống lại PD-1 hoặc PD-L1 có thể tăng cường hoạt tính kháng khối u của tế bào T với độ an toàn và khả năng dung nạp chấp nhận được. Pembrolizumab là một kháng thể đơn dòng mạnh, có chọn lọc, được nhân tính hóa, có ái lực cao với thụ thể PD-1 [32]. Mặc dù nó đã được chứng minh là có hiệu quả trong các khối u đặc khác (ung thư biểu mô của phổi, RCC, melanoma, ung thư biểu mô tế bào Merkle), có rất ít kinh nghiệm ở bệnh nhân NETs, chủ yếu cho thấy bệnh ổn định là đáp ứng tốt nhất [33].
Chiến lược điều trị
Nói chung, phẫu thuật là phương pháp điều trị đầu tiên cho các khối u nội tiết thần kinh khu trú, và có thể được xem xét để điều trị giảm nhẹ trong những trường hợp di căn hoặc ở mức độ gianh giới. Các phương pháp điều trị dựa trên bằng chứng được sử dụng gần đây cho GEP NET G1 và G2 tiên tiến bao gồm các đồng phân somatostatin (SSA), chất ức chế mTOR Everolimus, chất ức chế tyrosine kinase Sunitinib, PRRT và các liệu pháp nhắm mục tiêu tại gan cho những khối u di căn không thể cắt bỏ. Để kiểm soát triệu chứng ở bệnh tiến triển, SSA là liệu pháp chính, tiếp theo là bổ sung Ethyl telotristat ở bệnh nhân mắc hội chứng carcinoid không kiểm soát và các phương thức điều trị khác tùy theo đặc điểm bệnh cụ thể. Inbal Uri và Simona Grozinsky-Glasberg, trong bài tổng kết của mình, lần đầu tiên đưa ra một phác đồ điều trị dành cho các trường hợp GEP NENs tiến triển (Lược đồ 1) [34].
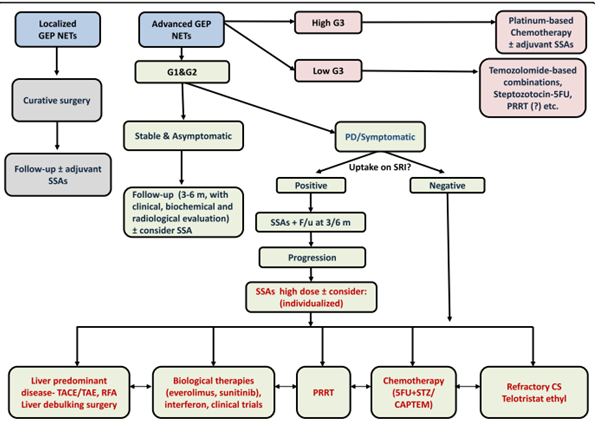
Lược đồ 1. Phác đồ tổng quát đối với GEP NENs nói chung và GEP NENs tiến triển của Inbal Uri và Simona Grozinsky [34]
Trong hướng dẫn điều trị của mình, Hiệp hội ung thư châu Âu (European Society for Medical Oncology – ESMO) cũng đã đưa ra khuyến cáo đối với giai đoạn bệnh tiến triển, nhưng mới chỉ áp dụng đối với NENs ruột non (small instestinal NENs – siNENs) và NENs của tụy (pancreatic NENs – pNENs) (Lược đồ 2) [35].

Lược đồ 2. Phác đồ điều trị bệnh tiến triển với siNENs, pNENs và NEC [35]
Xét riêng với nhóm bệnh nhân NENs G3, bao gồm hai nhóm nhỏ là NETs G3 và NECs G3, Anja Rinke và Thomas M. Gress trong bài viết tổng kết của mình cũng đã đưa ra một phác đồ điều trị cụ thể, trong đó, hóa trị vẫn là phương pháp điều trị đầu tiên với bệnh nhân NENs G3 giai đoạn tiến triển/di căn, tuy nhiên phác đồ hóa chất đối với hai nhóm NETs G3 và NECs G3 có sự khác nhau (Lược đồ 3) [36].

Lược đồ 3. Phác đồ điều trị với NENs G3
Kết luận
Vì các phương pháp điều trị truyền thống thường tạo ra sự ổn định khối u trong một khoảng thời gian giới hạn, nên có một nỗ lực lớn trong việc phát triển các phương pháp tiếp cận mới để khắc phục tình trạng kháng thuốc liên quan đến điều trị ở những bệnh nhân mắc NET tiến triển. Số lượng tương đối nhỏ bệnh nhân được đưa vào các nghiên cứu lâm sàng, cũng như diễn biến bệnh tương đối chậm, gây khó khăn cho việc đánh giá tỷ lệ đáp ứng với các liệu pháp mới và ảnh hưởng của chúng đối với khả năng sống còn. Vẫn còn nhiều nhu cầu chưa được đáp ứng trong kho vũ khí điều trị của NET (ví dụ: trình tự tối ưu của các phương thức điều trị, thăm dò và xác nhận các dấu ấn sinh học khác nhau, v.v.). Tuy nhiên, những hiểu biết mới về sự thay đổi phân tử của các khối u nội tiết thần kinh cuối cùng sẽ cải thiện sự hiểu biết về độ phức tạp của chúng, tạo điều kiện cho một phương pháp tiếp cận được cá nhân hóa và một phương pháp điều trị thành công cho từng bệnh nhân NET, trong tương lai gần.
Tài liệu tham khảo
1. Wang R., Zheng-Pywell R., Chen H.A., et al. (2019). Management of Gastrointestinal Neuroendocrine Tumors. Clin Med Insights Endocrinol Diabetes, 12.
2. Cives M. and Strosberg J. (2014). An update on gastroenteropancreatic neuroendocrine tumors. Oncol Williston Park N, 28(9), 749–756, 758.
3. Tsikitis V.L., Wertheim B.C., and Guerrero M.A. (2012). Trends of Incidence and Survival of Gastrointestinal Neuroendocrine Tumors in the United States: A Seer Analysis. J Cancer, 3, 292–302.
4. Dasari A., Shen C., Halperin D., et al. (2017). Trends in the Incidence, Prevalence, and Survival Outcomes in Patients With Neuroendocrine Tumors in the United States. JAMA Oncol, 3(10), 1335–1342.
5. Yao J.C., Hassan M., Phan A., et al. (2008). One hundred years after “carcinoid”: epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol Off J Am Soc Clin Oncol, 26(18), 3063–3072.
6. Rinke A., Müller H.-H., Schade-Brittinger C., et al. (2009). Placebo-controlled, double-blind, prospective, randomized study on the effect of octreotide LAR in the control of tumor growth in patients with metastatic neuroendocrine midgut tumors: a report from the PROMID Study Group. J Clin Oncol Off J Am Soc Clin Oncol, 27(28), 4656–4663.
7. Rinke A., Wittenberg M., Schade-Brittinger C., et al. (2017). Placebo-Controlled, Double-Blind, Prospective, Randomized Study on the Effect of Octreotide LAR in the Control of Tumor Growth in Patients with Metastatic Neuroendocrine Midgut Tumors (PROMID): Results of Long-Term Survival. Neuroendocrinology, 104(1), 26–32.
8. Caplin M.E., Pavel M., Ćwikła J.B., et al. (2014). Lanreotide in Metastatic Enteropancreatic Neuroendocrine Tumors. N Engl J Med, 371(3), 224–233.
9. Strosberg J.R., Halfdanarson T.R., Bellizzi A.M., et al. (2017). The North American Neuroendocrine Tumor Society Consensus Guidelines for Surveillance and Medical Management of Midgut Neuroendocrine Tumors. Pancreas, 46(6), 707–714.
10. Kölby L., Persson G., Franzén S., et al. (2003). Randomized clinical trial of the effect of interferon alpha on survival in patients with disseminated midgut carcinoid tumours. Br J Surg, 90(6), 687–693.
11. Yao J.C., Guthrie K.A., Moran C., et al. (2017). Phase III Prospective Randomized Comparison Trial of Depot Octreotide Plus Interferon Alfa-2b Versus Depot Octreotide Plus Bevacizumab in Patients With Advanced Carcinoid Tumors: SWOG S0518. J Clin Oncol Off J Am Soc Clin Oncol, 35(15), 1695–1703.
12. Pavel M.E., Baum U., Hahn E.G., et al. (2006). Efficacy and tolerability of pegylated IFN-alpha in patients with neuroendocrine gastroenteropancreatic carcinomas. J Interferon Cytokine Res Off J Int Soc Interferon Cytokine Res, 26(1), 8–13.
13. Kulke M.H., Hörsch D., Caplin M.E., et al. (2017). Telotristat Ethyl, a Tryptophan Hydroxylase Inhibitor for the Treatment of Carcinoid Syndrome. J Clin Oncol Off J Am Soc Clin Oncol, 35(1), 14–23.
14. Anthony L.B., Kulke M.H., Caplin M.E., et al. (2019). Long-Term Safety Experience with Telotristat Ethyl Across Five Clinical Studies in Patients with Carcinoid Syndrome. The Oncologist, 24(8), e662–e670.
15. Yao J.C., Fazio N., Singh S., et al. (2016). Everolimus for the treatment of advanced, non-functional neuroendocrine tumours of the lung or gastrointestinal tract (RADIANT-4): a randomised, placebo-controlled, phase 3 study. Lancet Lond Engl, 387(10022), 968–977.
16. Pavel M.E., Singh S., Strosberg J.R., et al. (2017). Health-related quality of life for everolimus versus placebo in patients with advanced, non-functional, well-differentiated gastrointestinal or lung neuroendocrine tumours (RADIANT-4): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol, 18(10), 1411–1422.
17. Anthony L.B., Pavel M.E., Hainsworth J.D., et al. (2015). Impact of Previous Somatostatin Analogue Use on the Activity of Everolimus in Patients with Advanced Neuroendocrine Tumors: Analysis from the Phase III RADIANT-2 Trial. Neuroendocrinology, 102(1–2), 18–25.
18. Wiedmann M.W. and Mössner J. (2012). Safety and efficacy of sunitinib in patients with unresectable pancreatic neuroendocrine tumors. Clin Med Insights Oncol, 6, 381–393.
19. Kulke M.H., Lenz H.-J., Meropol N.J., et al. (2008). Activity of sunitinib in patients with advanced neuroendocrine tumors. J Clin Oncol Off J Am Soc Clin Oncol, 26(20), 3403–3410.
20. Severi S., Grassi I., Nicolini S., et al. (2017). Peptide receptor radionuclide therapy in the management of gastrointestinal neuroendocrine tumors: efficacy profile, safety, and quality of life. OncoTargets Ther, 10, 551–557.
21. Kwekkeboom D.J., Krenning E.P., Lebtahi R., et al. (2009). ENETS Consensus Guidelines for the Standards of Care in Neuroendocrine Tumors: peptide receptor radionuclide therapy with radiolabeled somatostatin analogs. Neuroendocrinology, 90(2), 220–226.
22. Strosberg J., El-Haddad G., Wolin E., et al. (2017). Phase 3 Trial of 177Lu-Dotatate for Midgut Neuroendocrine Tumors. N Engl J Med, 376(2), 125–135.
23. Okusaka T., Ueno H., Morizane C., et al. (2015).Cytotoxic chemotherapy for pancreatic neuroendocrine tumors.J Hepato-Biliary-Pancreat Sci, 22(8), 628–633.
24. Sun W., Lipsitz S., Catalano P., et al. (2005). Phase II/III study of doxorubicin with fluorouracil compared with streptozocin with fluorouracil or dacarbazine in the treatment of advanced carcinoid tumors: Eastern Cooperative Oncology Group Study E1281. J Clin Oncol Off J Am Soc Clin Oncol, 23(22), 4897–4904.
25. Medley L., Morel A.N., Farrugia D., et al. (2011). Phase II study of single agent capecitabine in the treatment of metastatic non-pancreatic neuroendocrine tumours. Br J Cancer, 104(7), 1067–1070.
26. Yamaguchi T., Machida N., Morizane C., et al. (2014). Multicenter retrospective analysis of systemic chemotherapy for advanced neuroendocrine carcinoma of the digestive system. Cancer Sci, 105(9), 1176–1181.
27. Lu Y., Zhao Z., Wang J., et al. (2018). Safety and efficacy of combining capecitabine and temozolomide (CAPTEM) to treat advanced neuroendocrine neoplasms: A meta-analysis. Medicine (Baltimore), 97(41), e12784.
28. Welin S., Sorbye H., Sebjornsen S., et al. (2011). Clinical effect of temozolomide-based chemotherapy in poorly differentiated endocrine carcinoma after progression on first-line chemotherapy. Cancer, 117(20), 4617–4622.
29. Ribeiro M.J.M., Alonso T., Gajate P., et al. (2018). Huge recurrent gastric neuroendocrine tumor: a second-line chemotherapeutic dilemma. Autopsy Case Rep, 8(1), e2018005.
30. Dahan L., Bonnetain F., Rougier P., et al. (2009). Phase III trial of chemotherapy using 5-fluorouracil and streptozotocin compared with interferon alpha for advanced carcinoid tumors: FNCLCC-FFCD 9710. Endocr Relat Cancer, 16(4), 1351–1361.
31. Kulke M.H., Shah M.H., Benson A.B., et al. (2015). Neuroendocrine tumors, version 1.2015.J Natl Compr Cancer Netw JNCCN, 13(1), 78–108.
32. Patnaik A., Kang S.P., Rasco D., et al. (2015). Phase I Study of Pembrolizumab (MK-3475; Anti-PD-1 Monoclonal Antibody) in Patients with Advanced Solid Tumors. Clin Cancer Res Off J Am Assoc Cancer Res, 21(19), 4286–4293.
33. Pavel M.E. and Sers C. (2016). WOMEN IN CANCER THEMATIC REVIEW: Systemic therapies in neuroendocrine tumors and novel approaches toward personalized medicine. Endocr Relat Cancer, 23(11), T135–T154.
34. Uri I. and Grozinsky-Glasberg S. (2018). Current treatment strategies for patients with advanced gastroenteropancreatic neuroendocrine tumors (GEP-NETs). Clin Diabetes Endocrinol, 4(1), 16.
35. Pavel M., Öberg K., Falconi M., et al. (2020). Gastroenteropancreatic neuroendocrine neoplasms: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up†. Ann Oncol, 31(7), 844–860.
36. Rinke A. and Gress T.M. (2017). Neuroendocrine Cancer, Therapeutic Strategies in G3 Cancers.Digestion, 95(2), 109–114.
 UNG THƯ HỌC
UNG THƯ HỌC




Rất cám ơn bài tổng hợp chi tiết của BS Bình ạ!
PL