ĐẶT VẤN ĐỀ
Khối tân sản thần kinh nội tiết (Neuroendocrine neoplasms – NENs) là những tổ chức tân sản có nguồn gốc từ hệ thống tế bào thần kinh nội tiết, có thể lành tính hoặc ác tính [1]. Dựa về độ ác tính, NENs được chia làm 2 nhóm: U thần kinh nội tiết (neuroendocrine tumors – NETs) và ung thư thần kinh nội tiết (neuroendocrine carcinomas – NECs). Theo vị trí nguyên phát, chiếm tỷ lệ cao nhất là NENs hệ tiêu hóa (62%) [2], và trong nhóm u nguyên phát hệ tiêu hóa, NENs trực tràng chiếm tỷ lệ 15.2% [3].
Ngày nay, với sự phát triển của các công cụ chẩn đoán sớm như siêu âm, siêu âm nội soi, tỷ lệ phát hiện sớm bệnh tăng lên đáng kể, tương ứng với đó là các phương pháp can thiệp và điều trị ít xâm lấn như nội soi khoét niêm mạc kinh điển (endoscopic mucosal resection – EMR) và cải tiến (modifed EMR hay m-EMR) hoặc khoét dưới niêm mạc (endoscopic submucosal dissection – ESD). Tuy nhiên, trong phần lớn các trường hợp, phẫu thuật vẫn là phương pháp điều trị chính.
Về phẫu thuật, tùy vị trí cúng như kích thước khối u, mà có phương pháp điều trị khác nhau, như phẫu thuật cắt trước (Anterior Resection) hoặc cắt cụt trực tràng đường bụng tầng sinh môn (Abdominoperineal Resection-APR) [4]. Việc điều trị tiền phẫu trong những trường hợp giai đoạn muộn (di căn xa hoặc xâm lấn tại chỗ) còn chưa có tiêu chuẩn thống nhất và mới chỉ được báo cáo dưới dạng các ca lâm sàng hoặc các nghiên cứu mô tả [5], [6].
DỊCH TỄ HỌC
Theo số liệu của SEER (the Surveillance, Epidemiology and End Results), tỷ lệ mắc của NENs đại trực tràng đang tăng lên trong thời gian gần đây, chiếm 29% tổng số ca NENs hệ tiêu hóa, tính riêng trực tràng là 15.2%, qua đó trở thành vị trí mắc chiếm tỷ lệ cao nhất, cao hơn khá nhiều so với vị trí hay gặp thứ 2 là ruột non [3].
Tại châu Âu, theo các nghiên cứu tiến hành tại Anh và Áo, trực tràng lần lượt là vị trí hay gặp thứ 5 và thứ 4 với tỷ lệ 8% và 14% [7], [8]. Trong khi đó, tại châu Á, theo nghiên cứu của Ito và cộng sự, tỷ lệ này lên đến 56% [9]. Nghiên cứu của Modlin và cộng sự cũng cho thấy tỷ lệ mắc chiếm ưu thế ở nhóm gốc Á tại Hoa Kỳ [10]. Điều này gợi ý đến những yếu tố ảnh hưởng có khuynh hướng di truyền, ngoài ra có thể do các yếu tố liên quan đến sàng lọc và phát hiện sớm của từng hệ thống y tế [11].
Về giới tính, NENs trực tràng hay gặp chủ yếu ở nam giới, thời gian chẩn đoán thường ở nhóm 60 tuổi [12], [13].
TRIỆU CHỨNG HỌC
Khoảng 40% trường hợp bệnh được phát hiện tình cờ qua nội soi đại tràng sigma và nội soi đại tràng. Ngoài ra, các triệu chứng thường không đặc hiệu, bao gồm thay đổi thói quen đại tiện, đại tiện phân máu, hội chứng trực tràng (bao gồm mót rặn, khó chịu và đau) và gầy sút cân [14].
Rất hiếm khi NENs trực tràng biểu hiện triệu chứng của hội chứng Carcinoid. Các triệu chứng gợi ý di căn bao gồm đau bụng hạ sườn phải, gan to, ngủ gà, vã mồ hôi, chán ăn và hội chứng cận u. Tắc ruột hiếm khi xảy ra, thường gặp với các khối u vị trí trực tràng – sigma và giai đoạn xâm lấn muộn. 75 – 85% trường hợp u khú trú tại chỗ vào thời điểm chẩn đoán, trong khi chỉ có 2 – 8% phát hiện bệnh khi đã có di căn xa [15]. Theo số liệu của SEER từ 1973 đến 2004, 4% có xâm lấn tại chỗ và 5% có di căn xa. Tuy nhiên, theo một nghiên cứu khác của Nhật Bản, 30% có xâm lấn tại chỗ và 8% có di căn xa tại thời điểm chẩn đoán [9]
CHẨN ĐOÁN
Nội soi
Về đại thể, NENs thường có dạng nhỏ, không cuống, dưới niêm mạc bao phủ bởi niêm mạc biến đổi màu vàng [16]. Có thê gặp một số hình thái không điển hình về hình dạng (bán cầu hoặc nhú dạng loét), màu sắc (xung huyết) và thay đổi bề mặt (lõm, hoại tử và loét), thường phối hợp với di căn [17].
Nội soi đại trực tràng toàn bộ được khuyến cáo nhằm tránh bỏ sót tổn thương NENs hoặc các khối ung thư biểu mô đồng thời ở đại tràng [18].
Siêu âm nội soi trực tràng (Rectal ultrasound – RUS)
Đây là phương pháp cận lâm sàng hữu hiệu nhằm đánh giá kích thước, độ xấm lấn thành và di căn hạch lân cận trực tràng, từ đó đưa ra phác đồ điều trị chính xác [18]. Một nghiên cứu của Kobayashi và cộng sự đánh giá siêu ấm bằng ống siêu âm đại trực tràng (echocolonoscopes) trên 21 bệnh nhân và đầu dò siêu âm (ultrasonic probes) trên 32 bệnh nhân. Kết quả cho thấy, NENs trực tràng có dạng các khối được phân định rõ ràng, đồng nhất, đẳng lập hoặc giảm âm, độ xâm lấn thành được xác định chính xác trên tất cả các khối u (xâm lấn tới lớp dưới niêm mạc chiếm 49/52 trường hợp). RUS có khả năng xác định chính xác mức độ xâm lấn thành với những khối u đường kính nhỏ tới khoảng 2 mm [19]. Hai nghiên cứu khác cũng cho thấy khả năng chẩn đoán chính xác độ xâm lấn thành của RUS lần lượt là 91% và 100% [20], [21].
Chụp cắt lớp vi tín (Computed tomography – CT) và cộng hưởng từ (Magneticresonance imaging – MRI)
Chụp cắt lớp vi tính có vai trò đánh giá xâm lấn khu vực và di căn hạch, Tỷ lệ xác định chính xác di căn gan của CT là 81%. Đặc điểm hình ảnh trên CT đối với di căn hạch của NENs cũng tương tự với các dạng tổn thương ác tính khác, mạc dù độ ngấm thuốc có thể rõ ràng hơn [22].
Cộng hưởng từ tỏ ra ưu thế hơn trong chẩn đoán di căn gan và thường được sử dụng khi hình ảnh khối u trên CT còn nghi ngờ [11], [18]. Khuyến cáo của ENETS sử dụng CT/MRI đối với khối u kích thước > 10 mm, khi có nghi ngờ di căn hoặc tái phát [18]. Trong khi đó, khuyến cáo của NANETS không khuyến cáo sử dụng hai phương pháp này với những khối u có kích thước nhỏ hơn 20 mm và mới khu trú tại lớp niêm mạc – dưới niêm mạc [23].
Chụp nhấp nháy đồ – Xạ hình (Scintigraphic scanning – Octreoscan)
Chup nhấp nháy đồ với đồng vị phóng xạ gắn trên phân tử Somatostatin được dùng để xác định các tổ chức chứa receptor Somatostatin. Phương pháp này hay được sử dụng để chẩn đoán di căn [18]. Xác định khối u nguyên phát tại trực tràng với trạng thái hoạt động thông thường rất khó khăn [24]. Đặc biệt với các khối u thần kinh nội tiết đại trực tràng phân độ cao thường âm tính với Octreotide gắn Indium-111. Đối với những khối u âm tính với Octreotide, thì kỹ thuật ghi hình bằng bức xạ positron (Positron emission tomography – PET) có thể được sử dụng [18].
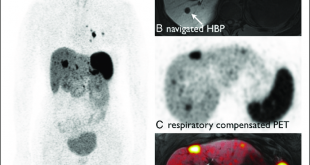
Kỹ thuật ghi hình bằng bức xạ positron (Positron emission tomography – PET)
FDG PET thường hữu ích đối với các khối u thần kinh nội tiết đại trực tràng phân độ cao/biệt hóa kém. Gallium-68 DOTA octreotide(ate) PET là phương pháp chẩn đoán hình ảnh còn chưa phổ biến, có độ nhạy cảm cao hơn so với xạ hình với indium-111 Octreotide [25].
Tóm lại, đối với một trường hợp nghi ngờ khối u trực tràng, các phương tiện chẩn đoán hình ảnh tối thiểu cần sử dụng bao gồm soi đại trực tràng kèm sinh thiết, CT ngực/bụng/chậu có tiêm thuốc cản quang. Với u trực tràng, cần thực hiện siêu âm nội soi trực tràng và MRI tiểu khung. Với các khối u < 10 mm, được cắt nội soi và có chỉ số Ki-67 thấp, không cần thiết phải đánh giá giai đoạn bệnh cũng như theo dõi sau mổ [18].
Các dấu ấn hóa học
Định lượng Chromagranin A máu là dấu ấn quan trọng đối với nhiều loại u thần kinh nội tiết nhưng thường hạn chế sử dụng đối với NENs trực tràng chưa di căn. [11]. Đây là phương pháp thường được áp dụng để đánh giá di căn, hoặc theo dõi sau mổ triệt căn đối với các khối u giai đoạn II và III [23]. Định lượng 5- hydroxyindoleacetic acid (5-HIAA) nước tiểu được sử dụng với những khối u tiết Serotonin [18].
Một số chất chỉ điểm của UTKNT đã được biết đến: chromogranin, synaptophysin, protein 9.5, phân tử gắn bề mặt tế bào nội tiết (NCAM/CD56), enolase thần kinh, và Leu 7. Trong đó Chromogranin A và Synaptophysin là 2 chất chỉ điểm u phổ biến nhất để khẳng định tính chất nột tiết của các tế bào u. Mặc dù là một chất chỉ điểm UTKNT quan trọng, Chromogranin A đôi khi biểu hiện âm tính đối với những dạng NETs mà các tế bào chứa ít túi tiết [26]. Tương tự, đối với NECs, sự biểu hiện của Chromogranin A thường yếu và không tuyệt đối [27]. Bên cạnh đó, với NENs đoạn ruột sau, mức độ biểu hiện của Chromogranin A cũng thường yếu hơn, mà ở đây thường biểu hiện Chromogranin B [26]. Synaptophysin là một thành phần của các túi synap và thường có mặt ở các tế bào thần kinh và thần kinh nội tiết. Không như Chromogranin A, Synaptophysin thường biểu hiện mạnh với những nhóm NENs độ ác tính cao [28].
Marker hóa mô miễn dịch đặc trưng theo cơ quan: CDX2, PAX8, PDX1, ISL-1. Trong những trường hợp di căn gan, điều quan trọng là cần tìm được vị trí tổn thương nguyên phát. Đôi khi, triệu chứng cơ năng, lâm sàng, chẩn đoán hình ảnh không thể giúp ta chẩn đoán chính xác vị trí u nguyên phát, một số chất chỉ điểm hóa mô miễn dịch có thể được sử dụng. Tổng hợp từ nhiều nghiên cứu cho thấy, các chất chỉ điểm miễn dịch như Thyroid transcription factor 1 (TTF1), Caudal Type Homeobox 2 (CDX2), ISL LIM Homeobox 1 (ISL-1), Pax8, và pancreatic and duodenal homeobox 1 (PDX1) có thể được sử dụng phục vụ mục tiêu này, nhằm phân biệt vị trí UTKNT biệt hóa cao nguồn gốc phổi, đường tiêu hóa và tụy (Bảng 1) [29], [30], [31], [32].

Trong một nghiên cứu khác của Yang và cộng sự, với ba chất chỉ điểm miễn dịch là TTF1, CDX2 và ISL1, có độ nhạy lần lượt là 81%, 89%, và 63%, độ đặc hiệu lần lượt là 100%, 94%, và 100% trong việc phân nhóm NENs di căn gan thành 3 nhóm tổn thương nguyên phát: phổi, ruột non và tụy/ trực tràng [33]. Gần đây, Yang và cộng sự tiếp tục đưa ra NK2 homeobox 2 (NKX2.2), như một chất có vai xác định vị trí tổn thương nguyên phát, theo đó, NKX2.2 cho thấy độ nhạy cáo hơn CDX2 và PDX1 trong việc xác định nguồn gốc của NENs biệt hóa cao phân tích trên 98 trường hợp [34].
TÀI LIỆU THAM KHẢO
1. Wang R., Zheng-Pywell R., Chen H.A., et al. (2019). Management of Gastrointestinal Neuroendocrine Tumors. Clin Med Insights Endocrinol Diabetes, 12.
2. Oronsky B., Ma P.C., Morgensztern D., et al. (2017). Nothing But NET: A Review of Neuroendocrine Tumors and Carcinomas. Neoplasia N Y N, 19(12), 991–1002.
3. Lawrence B., Gustafsson B.I., Chan A., et al. (2011). The epidemiology of gastroenteropancreatic neuroendocrine tumors. Endocrinol Metab Clin North Am, 40(1), 1–18, vii.
4. Chablaney S., Zator Z.A., and Kumta N.A. (2017). Diagnosis and Management of Rectal Neuroendocrine Tumors. Clin Endosc, 50(6), 530–536.
5. Bruera G., Giuliani A., Romano L., et al. (2019). Poorly differentiated neuroendocrine rectal carcinoma with uncommon immune-histochemical features and clinical presentation with a subcutaneous metastasis, treated with first line intensive triplet chemotherapy plus bevacizumab FIr-B/FOx regimen: an experience of multidisciplinary management in clinical practice. BMC Cancer, 19(1), 960.
6. Conte B., George B., Overman M., et al. (2016). High-Grade Neuroendocrine Colorectal Carcinomas: A Retrospective Study of 100 Patients. Clin Colorectal Cancer, 15(2), e1-7.
7. Ellis L., Shale M.J., and Coleman M.P. (2010). Carcinoid tumors of the gastrointestinal tract: trends in incidence in England since 1971. Am J Gastroenterol, 105(12), 2563–2569.
8. Niederle M.B., Hackl M., Kaserer K., et al. (2010). Gastroenteropancreatic neuroendocrine tumours: the current incidence and staging based on the WHO and European Neuroendocrine Tumour Society classification: an analysis based on prospectively collected parameters. Endocr Relat Cancer, 17(4), 909–918.
9. Ito T., Sasano H., Tanaka M., et al. (2010). Epidemiological study of gastroenteropancreatic neuroendocrine tumors in Japan. J Gastroenterol, 45(2), 234–243.
10. Modlin I.M., Lye K.D., and Kidd M. (2003). A 5-decade analysis of 13,715 carcinoid tumors. Cancer, 97(4), 934–959.
11. Mandair D. and Caplin M.E. (2012). Colonic and rectal NET’s. Best Pract Res Clin Gastroenterol, 26(6), 775–789.
12. Yoon S.N., Yu C.S., Shin U.S., et al. (2010). Clinicopathological characteristics of rectal carcinoids. Int J Colorectal Dis, 25(9), 1087–1092.
13. Kim D.H., Lee J.H., Cha Y.J., et al. (2014). Surveillance strategy for rectal neuroendocrine tumors according to recurrence risk stratification. Dig Dis Sci, 59(4), 850–856.
14. Shebani K.O., Souba W.W., Finkelstein D.M., et al. (1999). Prognosis and survival in patients with gastrointestinal tract carcinoid tumors. Ann Surg, 229(6), 815–821; discussion 822-823.
15. Yao J.C., Hassan M., Phan A., et al. (2008). One hundred years after “carcinoid”: epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol Off J Am Soc Clin Oncol, 26(18), 3063–3072.
16. McDermott F.D., Heeney A., Courtney D., et al. (2014). Rectal carcinoids: a systematic review. Surg Endosc, 28(7), 2020–2026
17. Kim B.N., Sohn D.K., Hong C.W., et al. (2008). Atypical endoscopic features can be associated with metastasis in rectal carcinoid tumors. Surg Endosc, 22(9), 1992.
18. Caplin M., Caplin M., Sundin A., et al. (2012). ENETS Consensus Guidelines for the Management of Patients with Digestive Neuroendocrine Neoplasms: Colorectal Neuroendocrine Neoplasms. Neuroendocrinology, 95(0), 88–97.
19. Kobayashi K., Katsumata T., Yoshizawa S., et al. (2005). Indications of Endoscopic Polypectomy for Rectal Carcinoid Tumors and Clinical Usefulness of Endoscopic Ultrasonography. Dis Colon Rectum, 48(2), 285–291.
20. Park C.H., Cheon J.H., Kim J.O., et al. (2011). Criteria for decision making after endoscopic resection of well-differentiated rectal carcinoids with regard to potential lymphatic spread. Endoscopy, 43(9), 790–795.
21. Ishii N., Horiki N., Itoh T., et al. (2010). Endoscopic submucosal dissection and preoperative assessment with endoscopic ultrasonography for the treatment of rectal carcinoid tumors. Surg Endosc, 24(6), 1413–1419.
22. Sundin A., Vullierme M.-P., Kaltsas G., et al. (2009). ENETS Consensus Guidelines for the Standards of Care in Neuroendocrine Tumors: Radiological Examinations. Neuroendocrinology, 90(2), 167–183.
23. Anthony L.B., Strosberg J.R., Klimstra D.S., et al. (2010). The NANETS consensus guidelines for the diagnosis and management of gastrointestinal neuroendocrine tumors (nets): well-differentiated nets of the distal colon and rectum. Pancreas, 39(6), 767–774.
24. Kwekkeboom D., Krenning E.P., and de Jong M. (2000). Peptide receptor imaging and therapy. J Nucl Med Off Publ Soc Nucl Med, 41(10), 1704–1713.
25. Srirajaskanthan R., Kayani I., Quigley A.M., et al. (2010). The role of 68Ga-DOTATATE PET in patients with neuroendocrine tumors and negative or equivocal findings on 111In-DTPA-octreotide scintigraphy. J Nucl Med Off Publ Soc Nucl Med, 51(6), 875–882.
26. Lloyd R.V. (2003). Practical markers used in the diagnosis of neuroendocrine tumors. Endocr Pathol, 14(4), 293–301.
27. Rindi G., Villanacci V., and Ubiali A. (2000). Biological and molecular aspects of gastroenteropancreatic neuroendocrine tumors. Digestion, 62 Suppl 1, 19–26.
28. Rindi G., Klöppel G., Alhman H., et al. (2006). TNM staging of foregut (neuro)endocrine tumors: a consensus proposal including a grading system. Virchows Arch Int J Pathol, 449(4), 395–401.
29. Koo J., Mertens R.B., Mirocha J.M., et al. (2012). Value of Islet 1 and PAX8 in identifying metastatic neuroendocrine tumors of pancreatic origin. Mod Pathol Off J U S Can Acad Pathol Inc, 25(6), 893–901.
30. Scoazec J.-Y., Couvelard A., Monges G., et al. (2017). Professional Practices and Diagnostic Issues in Neuroendocrine Tumour Pathology: Results of a Prospective One-Year Survey among French Pathologists (the PRONET Study). Neuroendocrinology, 105(1), 67–76.
31. Konukiewitz B., Enosawa T., and Klöppel G. (2011). Glucagon expression in cystic pancreatic neuroendocrine neoplasms: an immunohistochemical analysis. Virchows Arch Int J Pathol, 458(1), 47–53.
32. Garbrecht N., Anlauf M., Schmitt A., et al. (2008). Somatostatin-producing neuroendocrine tumors of the duodenum and pancreas: incidence, types, biological behavior, association with inherited syndromes, and functional activity. Endocr Relat Cancer, 15(1), 229–241.
33. Yang Z., Klimstra D.S., Hruban R.H., et al. (2017). Immunohistochemical Characterization of the Origins of Metastatic Well-differentiated Neuroendocrine Tumors to the Liver. Am J Surg Pathol, 41(7), 915–922.
34. Yang M.X., Coates R.F., Ambaye A., et al. (2018). NKX2.2, PDX-1 and CDX-2 as potential biomarkers to differentiate well-differentiated neuroendocrine tumors. Biomark Res, 6(1), 15.
 UNG THƯ HỌC
UNG THƯ HỌC