ĐẶT VẤN ĐỀ
Ung thư đường mật là những khối u ác tính xuất phát từ biểu mô của hệ thống đường mật từ trong gan đến đường mật ngoài gan và đường mật phụ.
Theo vị trí giải phẫu ung thư đường mật được chia thành 3 nhóm: Ung thư túi mật, ung thư đường mật và ung thư bóng Vater. Ung thư đường mật lại được chia thành: Ung thư đường mật trong gan, ung thư đường mật vùng rốn gan (U Klatskin) và ung thư phần thấp ống mật chủ. Về mặt giải phẫu thì ống gan phải và trái là thuộc đường mật ngoài gan do vậy các khối u vùng rốn gan (u Klatskin) được xếp vào ung thư đường mật ngoài gan [1]. Như vậy ung thư đường mật trong gan là những khối u xuất phát từ đường mật của các phân thuỳ trở lên (sau chỗ phân chia thứ hai của cây đường mật ). Có nhiều cách gọi loại ung thư này: ung thư đường mật trong gan (intrahepatic cholangiocarcinoma – IHCC), ung thư đường mật ngoại vi (peripheral cholangicarcinoma – PCC) [1], [2]. Đây là loại ung thư không thường gặp, chỉ chiếm 5 -10 % khối ung thư gan nguyên phát và 10% tổng số ung thư đường mật chung, tuy vậy đây là nhóm ung thư phổ biến thứ hai trong số các ung thư nguyên phát tại gan [2], [3], [4].
Bài viết này chúng tôi xin được điểm lại một số nét chính về dịch tễ học, triệu chứng, chẩn đoán cũng như điều trị của loại ung thư này.
DỊCH TỄ HỌC – Bệnh nguyên và bệnh sinh
Ung thư đường mật trong gan có nguồn gốc từ quá trình viêm nhiễm mạn tính đường mật trong gan làm tổn thương đường mật gây quá sản biểu mô đường mật, nguồn gốc xuất hiện ung thư. Các nguyên nhân thường gặp của UTĐMTG gồm: viêm chít đường mật nguyên phát, bệnh đường mật bẩm sinh, sỏi trong gan, sán lá gan [5], [6]. Theo nghiên cứu của các tác giả Âu-Mỹ thì nguyên nhân thường gặp là do bệnh đường mật, ngược lại với nghiên cứu của các tác giả châu Á thì phần lớn do nhiễm trùng.
Kể từ khi Sane và MacCallum mô tả lần đầu tiên UTĐMTG kèm sỏi mật năm 1942, ngày càng có nhiều nghiên cứu thấy mối liên quan của 2 bệnh này: UTĐMTG chiếm 9% các trường hợp sỏi trong gan ở Nhật Bản, 5% ở Đài Loan, ngược lại 21% số UTĐMTG có sỏi trong gan kèm theo tại Nhật Bản và 66-80% ở Đài Loan [7]. Sán lá gan là nguyên nhân thường gặp tại khu vực đông nam Á: đặc biệt ở Thái Lan, 94% UTĐMTG là Opisthorchis viverrini, ở Hồng Kông và Hàn Quốc là Clonorchis sinensis [8].
PHÂN LOẠI UNG THƯ ĐƯỜNG MẬT TRONG GAN
Phân loại theo giải phẫu bệnh
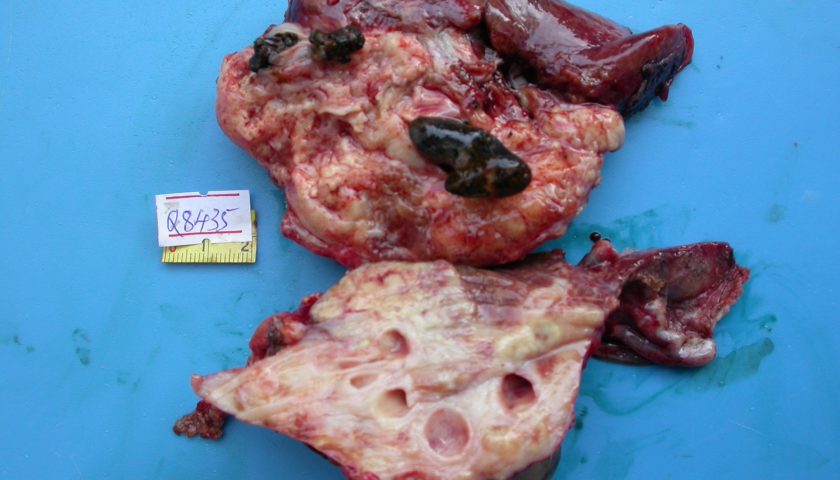
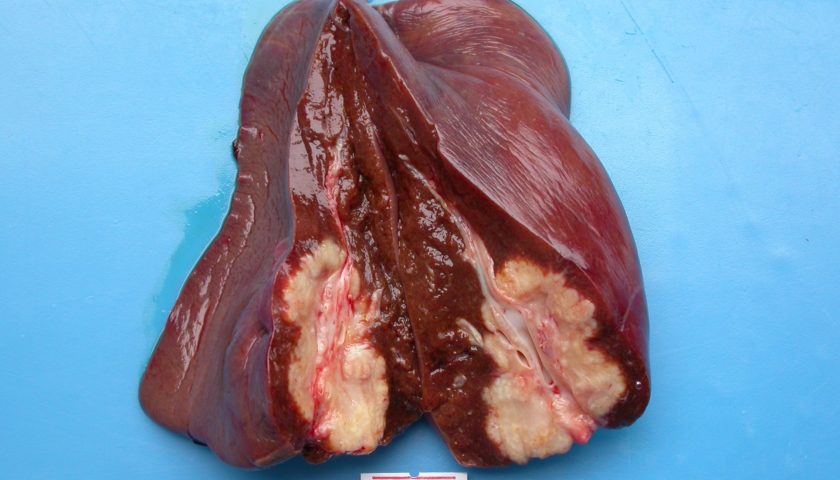
Đại thể
Có nhiều cách phân loại UTĐMTG dựa theo hình thái học và các thương tổn trong mổ
– Theo Eggel, cũng giống như ung thư biểu mô tế bào gan (Hepato Carcinoma Cellulaire-HCC) thì UTĐMTG cũng được chia làm 3 thể: thể nốt, thể khối và thể lan tỏa
– Weinbren và Mutum chia UTĐM thành 3 thể: thể nốt, thể xơ và thể nhú.
– Hiệp hội ung thư gan Nhật Bản, năm 1997 đã phân 3 loại thương tổn trong ung thư đường mật trong gan dựa trên đặc điểm phát triển của khối u: thể u, thể thâm nhiễm quanh đường mật, thể trong lòng đường mật [2].
Thể u thường nhầm với ung thư tế bào gan, giống ung thư tế bào gan là có xu hướng xâm lấn vào tĩnh mạch cửa, thường có di căn bên gan đối diện, tuy nhiên có điểm khác là ung thư đường mật trong gan thường tiến triển trên gan lành. Thể thâm nhiễm quanh đường mật thường do sỏi trong gan gây ra, có đặc điểm là tổn thương lan dọc theo cuống Glisson, do vậy hay có di căn hạch cuống gan. Còn thương tổn phát triển trong lòng đường mật là thương tổn đặc biệt, khối u xuất phát từ một điểm trên cây đường mật. Qua kết quả nghiên cứu của nhiều tác giả thì là đây là loại ung thư đường mật có tiên lượng tốt nhất, thời gian sống sau mổ dài (26-138 tháng) thậm chí đã có di căn hạch.
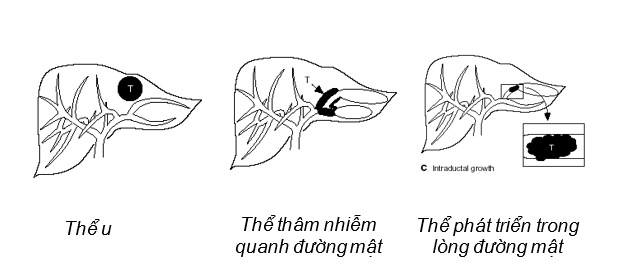
Hình 2: Các hình thái đại thể UTĐMTG
Vi thể
Là những ung thư biểu mô tuyến phát triển từ niêm mạc đường mật. U được cấu tạo bởi một lưới xơ mà trong đó chứa nhiều tuyến có các hình ảnh : ống, nhú hoặc các tế bào tự do (ung thư tế bào vảy, tế bào hạt..). Người ta gọi là các u tuyến khi trong mô có sự hiển diện của các tuyến này (bình thường tuyến chỉ nằm ở lớp niêm mạc), đồng thời các tế bào tuyến có hình ảnh tế bào ung thư (nhân lớn, kiềm tính, mất bào tương, nhiều lớp tế bào…). Khi các đặc trưng mô học của ung thư rõ ràng, số lượng tiêu bản đủ thì việc chẩn đoán mô học thường dễ dàng. Trái lại có thể rất khó xác định giữa ung thư với hình ảnh viêm đường mật hay giữa ung thư với loạn sản, quá sản. Trong viêm xơ đường mật mô liên kết của hệ thống đệm dày, xơ hoá cũng cho hình ảnh tương tự mô ung thư, lúc này những ống tuyến nằm sâu trong thành đường mật vì thế khó phân biệt với ung thư biệt hoá cao.
Bên cạnh các ung thư tuyến biệt hoá (ống, nhú, vách) hay tế bào tự do tuỳ theo vị trí phân bố của tế bào này còn có các dạng khác. Tất cả chúng đều là ung thư biểu mô. [3]
- Ung thư biểu mô tuyến (Adenocarcinoma) chiếm hơn 90%.
- Ung thư dạng biểu bì (Epidermoide).
- Ung thư nhầy dạng biểu bì chế nhầy (Mucoepidermoide).
- Ung thư cơ trơn (Leiomyosarcom).
- Ung thư biểu mô tuyến dạng nang (Cystadenocarcinoma).
- Ung thư tế bào hạt (Granular Cell).
- Ung thư tế bào vảy (Squamous).
- Ung thư biểu mô tuyến nhú.
- Thể hỗn hợp giữa UTĐM và ung thư tế bào gan( Hepato Cholangio Carcinoma)
Xâm lấn của các u này thường khu trú tại vùng, di căn ngoài gan rất hiếm, xâm lấn tại chỗ theo mạch máu, ống mật. Đối với xâm lấn vùng nổi trội và xâm lấn hạch (cuống gan). Xâm lấn tạng theo đường kế cận khá hiếm.

Ung thư biểu mô tuyến 
Ung thư biểu mô vẩy 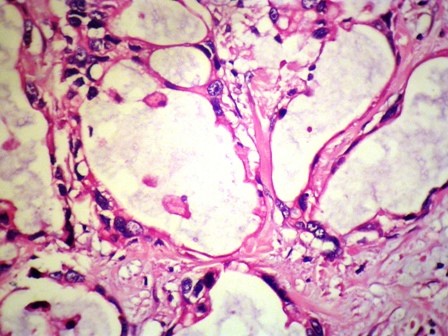
Ung thư biểu mô chế nhầy 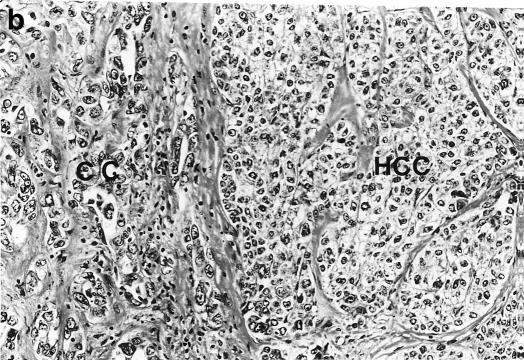
Ung thư thể hỗn hợp
Phân loại theo giai đoạn bệnh
Phân loại theo giai đoạn bệnh UTĐMTG trên thế giới hiện nay chủ yếu dựa theo phân loại của hiệp hội ung thư Hoa Kỳ (AJCC=American Joint Committee on Cancer) [9]:
– Đối với khối u (T):
- T1: khối u đơn độc, không có xâm lấn mạch;
- T2: khối u đơn độc có xâm lấn mạch hoặc nhiều khối u kích thước < 5cm;
- T3: đa khối u > 5cm hoặc u đã xâm lấn vào nhánh lớn của tĩnh mạch cửa hay tĩnh mạch gan;
- T4: khối u đã xâm nhiễm vào cơ quan xung quanh (ngoài túi mật) hay đã vỡ vào ổ phúc mạc.
– Đối với hạch di căn (N):
- N0: không có hạch di căn;
- N1: có hạch di căn..
– Đối với di căn tạng (M):
- M0: không có di căn xa;
- M1: có di căn xa.
Căn cứ vào T, N, M để xếp loại giai đoạn gồm 4 giai đoạn:
| Giai đoạn | T | N | M |
| I | T1 | N0 | M0 |
| II | T2 | N0 | M0 |
| IIIA | T3 | N0 | M0 |
| IIIB | T4 | N0 | M0 |
| IIIC | T bất kỳ | N1 | M0 |
| IV | T bất kỳ | N bất kỳ | M1 |
CHẨN ĐOÁN UNG THƯ ĐƯỜNG MẬT TRONG GAN
Với sự phát triển của khoa học kỹ thuật, và sự hiểu biết ngày càng đầy đủ về cơ chế bệnh sinh, chẩn đoán UTĐMTG không còn là vấn đề khó đối với y học ngày nay, tuy nhiên chẩn đoán ở giai đoạn sớm còn gặp nhiều khó khăn.
Triệu chứng lâm sàng
Ở giai đoạn sớm triệu chứng lâm sàng của UTĐMTG thường nghèo nàn và không đặc hiệu với các biểu hiện đau tức hạ sườn phải, ăn kém, gầy sút… [10]. Đa số bệnh nhân đến khám bệnh có biểu hiện đau tức hạ sườn phải, gầy sút, hoặc trong bệnh cảnh của tắc mật, nhiễm trùng đường mật do sỏi mật. Có khi bệnh nhân đến khám có biểu hiện của hội chứng vàng da tắc mật tăng dần trong trường hợp này thường bệnh đã ở giai đoạn muộn, khả năng phẫu thuật triệt căn là không cao [5], [8].
Hội chứng vàng da tắc mật:
- Trong UTĐMTG vàng da thường ở giai đoạn muộn, khi khối u to chèn ép vào đường mật ngoài gan hoặc có khi là hạch rốn gan to chèn ép vào cuống gan hoặc ống mật chủ, đặc điểm của vàng da trong UTĐMTG là vàng da tăng dần, kèm theo vàng da bệnh nhân có ngứa. Có nhiều trường hợp UTĐMTG nằm trong bệnh cảnh vàng da do sỏi mật và nhiễm trùng đường mật với các biểu hiện của đau hạ sườn phải, sốt , vàng da.
- Ngứa: thường gặp trong vàng da đậm, do ảnh hưởng của sắc tố mật.
- Phân bạc mầu: khi tắc mật hoàn toàn.
- Nước tiểu sẫm màu.
Đau hạ sườn phải: bệnh nhân thường đau tức âm ỉ, ít khi đau dữ dội.
Sốt : thường sốt nhẹ , sốt cao khi có nhiễm trùng đường mật kèm theo thường sốt nóng sốt rét
Hội chứng suy giảm chức năng gan: với các biểu hiện như xuất hiện sao mạch, bụng có dịch cổ trướng, xuất huyết dưới da….
Biểu hiện toàn thân:vàng da, gầy sút .. là những dấu hiệu khi ung thư ở giai đoạn muộn.
Triệu chứng thực thể:
- Gan to: Có thể gặp ở gan phải, gan trái hoặc gan to toàn bộ
- Túi mật to: ít gặp, túi mật to khi u gây chèn ép vào cuống gan và chỗ đổ của ống cổ túi mật, có thể gặp trong trường hợp hạch rốn gan to chèn ép vào ống mật chủ
- Dịch cổ trướng, tuần hoàn bàng hệ: khi u đã di căn phúc mạc [11]
- Thiếu máu: có nhiều mức độ tùy theo giai đoạn bệnh
Biến chứng vỡ khối u gây chảy máu trong ổ bụng có thể xảy ra, tuy nhiên hiếm gặp hơn so với ung thư tế bào gan nguyên phát, có thể lý giải do cấu trúc mô học giàu tổ chức đệm chắc chắn [12]. Bên cạnh đó giai đoạn muộn có thể gặp các biến chứng như hội chứng Budd – Chiari do xâm lấn tĩnh mạch trên gan hoặc di căn hạch gây chèn ép [13].
Triệu chứng cận lâm sàng
Chẩn đoán UTĐMTG phải tiến hành qua các bước thăm khám lâm sàng, các xét nghiệm sinh hóa, chức năng gan, chất chỉ điểm khối u, siêu âm, chụp cắt lớp vi tính, cộng hưởng từ và một số phương pháp chẩn đoán hình ảnh khác.
Các xét nghiệm sinh học.
– Các xét nghiệm sinh học ở giai đoạn sớm thường chưa có sự thay đổi , ở giai đoạn muộn được biểu hiện bằng hội chứng vàng da tắc mật, suy chức năng gan như tăng bilirubin, tỉ lệ prothrombin giảm, albumin máu giảm….. Trong trường hợp có viêm đường mật phối hợp thì thường có số lượng bạch cầu trong máu tăng cao.
– Chất chỉ điểm khối u: Khi khối u xuất hiện trong cơ thể thì bản thân khối u sẽ sản sinh ra những chất đặc biệt, các chất này sẽ đóng vai trò như chất chỉ điểm khối u. Năm 1979 Koprowski phát hiện ra chất chỉ điểm khối u CA 19-9 là một kháng nguyên liên kết ung thư khi tiêm kháng thể đơn dòng SW 1116 sản sinh bởi tế bào ung thư đại tràng trên chuột nhắt trắng. Kháng nguyên này dương tính trong UTĐM và một số bệnh lý khác, ngoài ra CEA, CA125, CA-195, CA-242, DU-PAN-2, IL-6 và trypsinogen-2…cũng được ứng dụng trên lâm sàng [14].
– Kháng nguyên CA 19-9 tăng cao, nhưng không chỉ tăng trong ung thư đường mật mà còn có thể tăng trong các trường hợp tắc mật lành tính. Chất chỉ điểm khối u không chỉ được sử dụng để phát hiện ung thư trên những bệnh nhân viêm xơ hoá đường mật mạn tính vì độ nhạy 89% và độ đặc hiệu 86% mà còn được sử dụng để theo dõi và phát hiện ung thư tái phát sau mổ [15], [16].
– Các xét nghiệm khác:
- Lấy mẫu qua da bởi kim hút tế bào có khẩu kính nhỏ hoặc kim sinh thiết có khẩu kính lớn.
- Qua ống soi lấy dịch mật hoặc dịch tụy để phân tích tế bào và tìm trứng sán và sán.
- Phương pháp lấy nội mạc bao gồm: chải mô, kìm bấm sinh thiết, rửa nòng.
- Tìm trứng sán và sán trong phân và hiệu giá kháng thể của phản ứng Elisa khi nghi ngờ có sán trong đường mật.
Chẩn đoán hình ảnh
Siêu âm: Trong ung thư đường mật, siêu âm có thể cung cấp các thông tin về vị trí, kích thước, cấu trúc âm của khối u [4]. Ngay cả khi không phát hiện được khối u thì siêu âm cũng cung cấp thông tin về vị trí và mức độ tắc nghẽn đường mật. Siêu âm còn có thể phát hiện huyết khối tĩnh mạch cửa, di căn hạch và di căn các tạng. Đây là ưu điểm của siêu âm so với nội soi hay chụp đường mật nhờ đó các nhà lâm sàng đánh giá đầy đủ hơn về bệnh để đưa ra phương pháp điều trị thích hợp [17]. Ngoài ra siêu âm còn hướng dẫn các thày thuốc lâm sàng tiến hành các thủ thuật như: chụp đường mật hay dẫn lưu đường mật qua da, siêu âm trong mổ xác định vị trí u, liên quan giữa u với các thành phần cuống cửa và tĩnh mạch trên để hạn chế tai biến trong mổ.
SA có thể thấy khối u chiếm tỷ lệ 21 – 47% các trường hợp. Hình ảnh các khối đồng âm với nhu mô gan chiếm 44 – 65%, tăng âm chiếm 33 – 35%, đầu trên có hình cong lõm (hình càng cua), cấu trúc âm này không kèm bóng cản [18]. Thành đường mật có thể bị phá huỷ và khối u phát triển ra xung quanh. Hình ảnh giãn đường mật phía trên là dấu hiệu gián tiếp và thường thấy. Tuy nhiên trong thể thâm nhiễm lan toả đường mật có thể thấy đường mật không giãn. Trường hợp u rốn gan gây dãn đường mật trong gan không gây dãn đường mật chính và không giãn túi mật, các khối u ở phía dưới chỗ đổ vào của ống túi mật sẽ gây giãn túi mật [17], [19].
Siêu âm có thể đánh giá sự xâm lấn thành đường mật và nhu mô gan của tổn thương ung thư với tỷ lệ 44%. Siêu âm có thể thấy hình ảnh huyết khối TMC hơn là động mạch gan, hiếm hơn nữa là khối hoại tử trong u [17], [18].
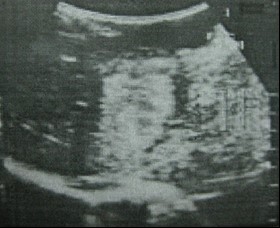
Khối tăng âm đồng nhất 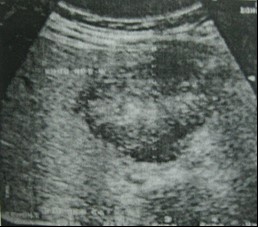
Khối hỗn hợp âm, bờ không đều
TÀI LIỆU THAM KHẢO
1. Chen M.F. (1999).
Peripheral cholangiocarcinoma (cholangiocellular carcinoma): clinical features, diagnosis and treatment. J Gastroenterol Hepatol, 14(12), 1144–1149.
2. Ohtsuka M., Ito H., Kimura F., et al. (2002).
Results of surgical treatment for intrahepatic cholangiocarcinoma and clinicopathological factors influencing survival. Br J Surg, 89(12), 1525–1531.
3. Fulcher A.S. and Sterling R.K. (2002).
Hepatic neoplasms: computed tomography and magnetic resonance features. J Clin Gastroenterol, 34(4), 463–471.
4. Lim J.H. (2004).
Cholangiocarcinoma: recent advances in imaging and intervention. Abdom Imaging, 29(5), 538–539.
5. Zimmermann A. (2017).
Intrahepatic Cholangiocarcinomas (ICCs). Tumors and Tumor-Like Lesions of the Hepatobiliary Tract: General and Surgical Pathology. Springer International Publishing, Cham, 549–586.
6. Kim H.J., Kim J.S., Joo M.K., et al. (2015).
Hepatolithiasis and intrahepatic cholangiocarcinoma: A review. World J Gastroenterol, 21(48), 13418–13431.
7. Yang J. and Yan L.-N. (2008).
Current status of intrahepatic cholangiocarcinoma. World J Gastroenterol WJG, 14(41), 6289–6297.
8. Chu K.-M., Lai E.C.S., Al-Hadeedi S., et al. (1997).
Intrahepatic Cholangiocarcinoma. World J Surg, 21(3), 301–306.
9. Huang J.L., Biehl T.R., Lee F.T., et al. (2004).
Outcomes after resection of cholangiocellular carcinoma. Am J Surg, 187(5), 612–617.
10. Dialogues L. Les Cancers des voies biliaires extra-hépatique… – Congrès français de chirurgie – Masson: 10-125.
11. Yamamoto N., Shiraki K., Yamanaka Y., et al. (2004).
Images of interest. Hepatobiliary and pancreatic: cholangiocarcinoma with chylous ascites. J Gastroenterol Hepatol, 19(12), 1417.
12. Chong R.W.W., Chung A.Y.F., Chew I.W.C., et al. (2006).
Ruptured peripheral cholangiocarcinoma with hemoperitoneum. Dig Dis Sci, 51(5), 874–876.
13. Kwon O.S., Jung D.W., Kim S.H., et al. (2007).
Distant skeletal muscle metastasis from intrahepatic cholangiocarcinoma presenting as Budd-Chiari syndrome. World J Gastroenterol, 13(22), 3141–3143.
14. Malaguarnera G., Giordano M., Paladina I., et al. (2011).
Markers of bile duct tumors. World J Gastrointest Oncol, 3(4), 49–59.
15. Dorandeu A., Raoul J.L., Siriser F., et al. (1997).
Carcinoma of the ampulla of Vater: prognostic factors after curative surgery: a series of 45 cases. Gut, 40(3), 350–355.
16. Nakamura S., Suzuki S., Sakaguchi T., et al. (1996).
Surgical treatment of patients with mixed hepatocellular carcinoma and cholangiocarcinoma. Cancer, 78(8), 1671–1676.
17. Bloom C.M., Langer B., and Wilson S.R. (1999).
Role of US in the Detection, Characterization, and Staging of Cholangiocarcinoma. RadioGraphics, 19(5), 1199–1218.
18. Wibulpolprasert B. and Dhiensiri T. (1992).
Peripheral cholangiocarcinoma: sonographic evaluation. J Clin Ultrasound JCU, 20(5), 303–314.
19. Lee N.W., Wong K.P., Siu K.F., et al. (1984).
Cholangiography in hepatocellular carcinoma with obstructive jaundice. Clin Radiol, 35(2), 119–123.
 UNG THƯ HỌC
UNG THƯ HỌC