Những nội dung chính
ĐẠI CƯƠNG
Ung thư biểu mô thận hay ung thư tế bào thận (renal cell carcinoma: RCC) chiếm khoảng 3% của toàn bộ các loại ung thư của người lớn và đại diện trên 90% các u ác tính ở thận. Bệnh này thường xuất hiện ở người lớn trên 50 tuổi với tỷ lệ nam giới nhiều gấp hai lần so với nữ giới. [1]
Những năm gần đây, các nghiên cứu sinh học phân tử cho thấy RCC có tính lẻ tẻ, chỉ khoảng 4% đến 6% là có tính di truyền (Lipworth và cộng sự, 2006; Schmidt và Linehan, 2016). Tỷ lệ mới mắc RCC đã tăng lên từ những năm 1970, trung bình 3% mỗi năm, chủ yếu liên quan đến việc sử dụng phổ biến hơn của siêu âm và CT (Decastro và McKiernan, 2008; Kummerlin và cộng sự, 2008). [2]
Việc phát hiện giai đoạn sớm đã dẫn đến khái niệm điều trị bảo tồn thận trong một số điều kiện nhất định. Tuy nhiên, trong số bệnh nhân có triệu chứng lúc đến khám thì một phần ba đã có di căn. Hơn nữa, gần một nửa bệnh nhân được phẫu thuật triệt để lại có dấu hiệu ung thư tiến triển. Vì vậy, đối với ung thư giai đoạn muộn, việc điều trị bằng các phương pháp miễn dịch đang được tập trung nghiên cứu để kéo dài cuộc sống của bệnh nhân. [1]
NGUYÊN NHÂN BỆNH SINH
RCC phát sinh chủ yếu từ các ống lượn gần, và điều này có lẽ đúng với tế bào sáng (clear cell) và nhú (papillary). Tuy nhiên, hiện nay chúng ta biết rằng các loại mô học khác của RCC, như tế bào kỵ màu (chromophobe) và ung thư biểu mô ống góp (collecting duct carcinoma), có nguồn gốc từ các thành phần xa của nephron (Moch và cộng sự, 2016; Pantuck và cộng sự, 2001a). [2]
Thuốc lá là yếu tố nguy cơ đáng chú ý trước tiên vì nghiện thuốc lá có nguy cơ mắc bệnh gấp hai lần so với người không hút thuốc lá (Yu, 1986). Tăng huyết áp và chứng béo phì cũng là những nguy cơ tiềm tàng.
Béo phì với nguy cơ tương đối tăng 1,07 cho mỗi đơn vị BMI (body mass index ) (Bagheri và cộng sự, 2016; Bhaskaran và cộng sự, 2014; Ito và cộng sự, 2017; Renehan và cộng sự, 2008). [2]
Đặc biệt các bệnh nhân thận đa nang bẩm sinh hay mắc phải trong suy thận mạn hay chạy thận nhân tạo chu kỳ hoặc bệnh tăng sinh dòng tế bào sau ghép thận cũng có tần số mắc RCC khá cao. [1]
Năm 1979, Cohen tìm thấy khuyết tật chuyển đoạn của nhiễm sắc thể 3p trong ung thư thận tế bào sáng. Latif, năm 1993, phát hiện gen VHL ở vùng p25 – p26 của nhiễm sắc thể 3, gây ra ung thư thận tế bào sáng cả hai thận trong bệnh Von Hippel – Lindau, Các biểu hiện chính bao gồm RCC, pheochromocytoma, u mạch võng mạc và hemangioblastomas của thân não, tiểu não hoặc tủy sống. RCC phát triển ở khoảng 50% bệnh nhân mắc bệnh VHL, khởi phát sớm (30 – 50 tuổi), hai bên và đa ổ (Kim và cộng sự, 2010; Schmidt và Linehan, 2016). [2]
GIẢI PHẪU BỆNH LÝ
Về đại thể, u xuất phát từ nhu mô thận, lớn dần và có thể có một bao giả. U có rất nhiều mạch máu nuôi dưỡng. Khi rạch khối u sẽ thấy màu sắc sặc sỡ vàng nâu hay lốm đốm do các vùng hoại tử chảy máu xen lẫn các đám vôi hóa. U dần phát triển ra ngoài bao thận, lan ra các lớp mỡ quanh thận, xâm lấn các tạng trong vùng.
Một đặc điểm độc đáo của RCC là khả năng xâm lấn hệ thống tĩnh mạch, 10% trường hợp, thường xuyên hơn bất kỳ ung thư nào khác (Schefft và cộng sự, 1978; Skinner và cộng sự, 1972). Chồi u có thể xâm lấn vào trong tĩnh mạch thận và tĩnh mạch chủ dưới (IVC) và lên cao đến tâm nhĩ phải (Novick và cộng sự, 1990), một số xâm lấn trực tiếp vào thành tĩnh mạch thận hoặc tĩnh mạch chủ, điều này tương quan với tiên lượng bệnh (Haddad và cộng sự, 2014; Schefft và cộng sự ., 1978; Skinner và cộng sự, 1972; Zini và cộng sự, 2008). [2]
Hiệp hội quốc tế chống ung thư giới thiệu năm thể loại sau đây:
- Ung thư thận tế bào sáng (ccRCC) chiếm khoảng 70% – 80% các trường hợp, có nguồn gốc từ ống lượn gần, thường có giới hạn rõ. Các tế bào tròn hay đa cạnh với bào tương sáng chứa nhiều glycogen và lipid. Loại ung thư này thường có khuyết đoạn ở NST 3p và có tiên lượng rất kém.

- Ung thư nhú thận (pRCC) chiếm khoảng 10% – 15% RCC, ung thư có thể xuất hiện ở hai bên thận. Cấu trúc vi thể có mô hình ống – nhú ưa kiềm và các tế bào được sắp xếp theo một trục xơ mạch hay xếp thành ống xen kẽ với mô thận bình thường. Gen được xác định là C – MET, một tiền oncogen ở nhiễm sắc thể 7q.
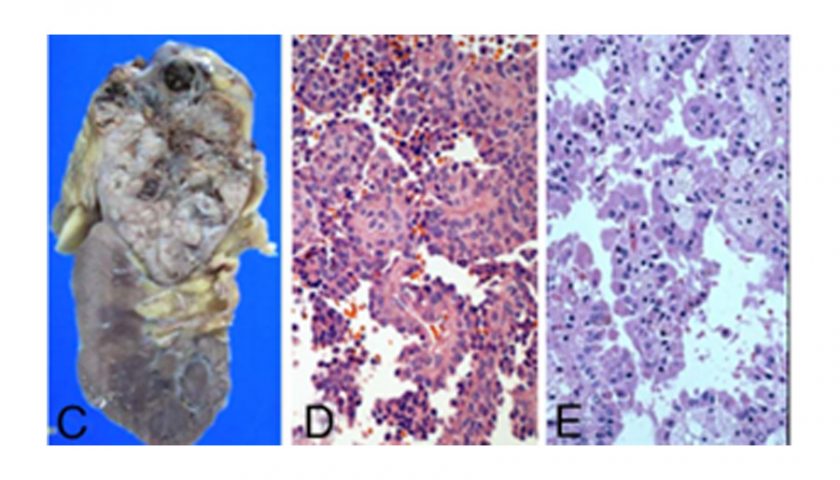
- Ung thư thận kỵ màu (Chromophobe RCC, chRCC) chiểm khoảng 3% – 5%, được Thoenes mô tả vào năm 1985, u có màu vàng nhạt, tương phẳng với các đám hoại tử xen lẫn với các dải xơ. . Mất NST Y, 1, 2, 6, 10, 13, 17 và 21 là những sự thay đổi gen đặc trưng. [2]

- Oncocytom thận chiếm khoảng 3% – 7% các trường hợp, thường đa số là lành tính, tuy nhiên các tế bào có thể thay đổi từ độ 1 đến độ 3 để trở thành ác tính.
- Ung thư ống góp Bellini chiếm 1% – 2% các trường hợp, có tiên lượng rất xấu.
CÁC GIAI ĐOẠN XÂM LẤN RCC
Có 2 cách phân chia u ác tế bào thận: theo phân loại của Robson và phân loại của Hiệp Hội Chống Ung Thư Quốc Tế (phân chia theo giai đoạn TNM).
- Phân loại Robson 1990 [2] :
Được áp dụng nhiều trong thực hành lâm sàng do tiện dụng: có 4 giai đoạn phát triển lâm sàng theo phân loại cổ điển:
| Giai đoạn | Mô tả |
| Giai đoạn I | U còn khu trú trong bao thận, chưa có dấu hiệu lâm sàng. |
| Giai đoạn II | U đã phá vỡ bao xơ thận lan đến lớp mỡ, nhưng vẫn chưa đến cân Gerota. |
| Giai đoạn III | |
| IIIa | U lan đến tĩnh mạch thận. |
| IIIb | Tế bào ung thư lan đến hạch bạch huyết. |
| IIIc | Lan đồng thời đến tĩnh mạch thận và hạch bạch huyết. |
| Giai đoạn IV | |
| IVa | U lan đến các tạng lân cận. |
| IVb | Di căn xa. |
2. Phân loại theo giai đoạn TNM [ 3 ]
| Hệ thống phân loại TNM | |||
| T | U nguyên phát. | ||
| TX | U nguyên phát không đánh giá được. | ||
| T0 | Không có bằng chứng của u nguyên phát. | ||
| T1 | U có kích thước lớn nhất <= 7 cm, giới hạn trong thận. | ||
| T1a | U <= 4 cm. | ||
| T1b | U > 4 cm nhưng <= 7 cm. | ||
| T2 | U có kích thước lớn nhất > 7 cm, giới hạn trong thận. | ||
| T2a | U > 7 cm nhưng <= 10cm. | ||
| T2b | U > 10 cm giới hạn trong thận, giới hạn trong thận. | ||
| T3 | U xâm lấn tĩnh mạch chính hoặc xâm lấn các mô quanh thận, nhưng chưa xâm lấn tuyến thượng thận cùng bên và vào cân Gerota. | ||
| T3a | U xâm lấn toàn bộ tĩnh mạch thận hoặc xâm lấn một phần cơ, hoặc xâm lấn mỡ quanh thận/ xâm lấn mỡ xoang thận, nhưng chưa ăn vào cân Gerota. | ||
| T3b | U xâm lấn nhiều vào tĩnh mạch chủ dưới cơ hoành. | ||
| T3c | U xâm lấn dầy vào tĩnh mạch chủ trên cơ hoành, hoặc xâm lấn vào thành tĩnh mạch chủ. | ||
| T4 | U xâm lấn qua cân Gerota (gồm xâm lấn trực tiếp qua tuyến thương thận cùng bên). |
| N | Hạch tại chỗ | |||
| NX | Hạch tại chỗ không phát hiện | |||
| N0 | Không di căn hạch tại chỗ | |||
| N1 | Di căn một hoặc nhiều hạch tại chỗ | |||
| M | Di căn xa | |||
| M0 | Không di căn xa | |||
| M1 | Di căn xa | |||
| pTNM phân chia giai đoạn | ||||
| GĐ I | T1 | N0 | M0 | |
| GĐ II | T2 | N0 | M0 | |
| GĐ III | T3 | N0 | M0 | |
| T1, T2, T3 | N1 | M0 | ||
| GĐ IV | T4 | Bất kì N | M0 | |
| Bất kì T | Bất kì N | M1 |
CHẨN ĐOÁN
- Tam chứng cổ điển: tiểu máu – đau hông lưng – khối u vùng hông lưng:
Là nhóm triệu chứng quan trọng, nhưng chỉ có 10% các trường hợp có đủ tam chứng này trên cùng một bệnh nhân.
- Tiểu máu : là triệu chứng rất hay gặp ( 80% trường hợp ) [1]. Tiểu máu đại thể, toàn dòng, không đau, không buốt khi đi tiểu. Nhưng khi tiểu máu nhiều, máu cục làm tắc nghẽn niệu quản sẽ xuất hiện cơn đau quặn thận. Tiểu máu đột ngột, thường tự khỏi tự nhiên rồi tái phát nhưng không rõ nguyên nhân.
- Đau hông lưng : Tính chất đau sẽ tùy theo giai đoạn của u, đau âm ỉ, lan ra trước hay lan xuống dưới do u phát triển xuống dưới làm căng bao thận. Có thể đau quặn thận khi có cục máu đông di chuyển xuống niệu quản làm tắc nghẽn niệu quản.
- Khối u vùng hông lưng : những trường hợp thăm khám được khối u thận thường là triệu chứng trễ của u, u đã lớn, tiến triển lâu ngày. Có thể nhìn thấy sự bất cân xứng của hai hố thắt lưng và các dấu hiệu chạm thận hay bập bềnh thận. Lúc thăm khám, nên nhẹ nhàng để tránh gây di căn ung thư.
Nghiệm pháp bập bềnh thận dương tính cho biết khối u còn di động, chưa xâm lấn xung quanh, là dấu hiệu tiên lượng tốt cho phẫu thuật
- Hội chứng cận ung: [1]
- Tăng hồng cầu thứ phát: 3-10%, do tăng sản xuất erythropoietin hoặc do thiếu oxy mô cục bộ tại thận
- Tăng canxi máu: 20%, do Peptide giống hormon cận giáp.
- Tăng HA: 40%, kháng trị, đáp ứng sau cắt thận, do tăng sản xuất Renin.
- Hội chứng Stauffer: 3-20%.
- Rối loạn chức năng gan không do di căn: tăng ALP, γGlobulin, Bilirubin, giảm Albumin, PT kéo dài
- Sốt, mệt mỏi, sụt cân, cải thiện sau cắt thận, do u tiết chất kích thích dòng đại thực bào.
- Hội chứng cận ung không trở về bình thường sau cắt thận có tiên lượng xấu.
- Triệu chứng di căn:
- Di căn hệ tĩnh mạch: đặc biệt di căn tĩnh mạch thận trái làm sớm giãn tĩnh mạch tinh trái, di căn tĩnh mạch chủ bụng gây giãn tĩnh mạch tinh phải và tuần hoàn bàng hệ bụng.
- Di căn gan: với nhân cứng, bụng báng, vàng da, suy gan, phù 2 chân. Ngược lại có một số trường hợp suy gan không phải do di căn nhưng tăng phosphatase kiềm, giảm bạch cầu, đau vùng gan, hoại tử tế bào gan. Đó là hội chứng giống di căn gan trong u thận.
- Di căn xương: gây các triệu chứng tại chỗ vùng xương.
- Di căn não cho các triệu chứng thần kinh
CẬN LÂM SÀNG
- Tổng phân tích nước tiểu :xác định tiểu máu đại thể, vi thể. Hồng cầu âm tính không phải là kết luận của chẩn đoán.
- Huyết học và sinh hoá
- Chức năng gan rối loạn: đôi khi khó phân biệt với u di căn gan trong hội chứng cận ung thư.
- Tốc độ máu lắng tăng hay giảm.
- Có thể đa hồng cầu hoặc thiếu máu
- Canxi máu, phosphate kiềm, chức năng thận. Mục đích để đánh giá chức năng thận tình trạng toàn thân và phát hiện các dấu hiệu của ” Hội chứng cận u ” [1]
- Các phương pháp chẩn đoán hình ảnh:
- Siêu âm bụng tổng quát :
- Chẩn đoán hình ảnh sử dụng đầu tiên, dễ sử dụng, không nguy hiểm, khả năng phát hiện u thận rất tốt, ngay cả u nhỏ, chưa biểu hiện lâm sàng. Siêu âm cho phép chẩn đoán các u đặc ở thận và các di căn vào tĩnh mạch thận, tĩnh mạch chủ, các hạch ở cuống thận.
- Siêu âm tổng quát phát hiện :
- Phát hiện được 85% u có kích thước > 3cm, tỷ lệ này £ 60% khi u có kích thước < 2cm [4]
- Hình ảnh tăng âm ( 48 % ), đồng âm ( 42%), giảm âm ( 10% ) đối với khối u thận. [4]
- Nang thận ác tính :
- Siêu âm thấy được nang nhiều vách ngăn, dày.
- Nốt sần vôi hóa.
- Xuất huyết trong nang hoặc nang hoại tử với hình ảnh giảm âm, Fluid – debris level.
- Chụp đường niệu tĩnh mạch ( UIV ):
- Siêu âm bụng tổng quát :
Ít được sử dụng vì những giới hạn của UIV so với CT scan bụng – chậu:
- Không phân biệt được hình ảnh nang và u thận là nhược điểm lớn.
- Vai trò chủ yếu trong UIV là quan sát chức năng thận đối bên. Đó là hình ảnh rất quan trọng khi quyết định cắt thận u.
- Khi thận câm không thể phân biệt được thận ứ nước và u.
- Không định được giai đoạn tiến triển của u, mức độ xâm lấn, hạch di căn.
- Hình ảnh thận và các đài thận và bể thận biến dạng do u xâm lấn chèn ép, lúc tiêm thuốc có thể thấy một khối vượt ra khỏi bờ ngoài của thận, có hình khuyết trong những phim chụp sau.

- Chụp cắt lớp vi tính ( CT scan ):
- Là cận lâm sàng cho phép xác định được tính chất của u và đánh giá sự xâm lấn của u rất quan trọng trong việc quyết định phương pháp điều trị u thận.
- Xác định được mức lành tính của nang và u ác bằng cách đo mật độ cản quang.
- Phân biệt được các giai đoạn tiến triển của u: đánh giá hạch di căn, các khối u di căn vào rốn thận, tĩnh mạch thân và tĩnh mạch chủ, tuyến thượng thận và các cơ quan lân cận.
- Chụp 2 phim bao gồm không có thuốc cản quang (NECT) và có thuốc cản quang mạch máu ( CECT) , cần phân tích được 4 mục tiêu: khối u , xâm lấn quanh thận, xâm lấn tĩnh mạch, xâm lấn hạch bạch huyết.
- CT scan tìm thấy hình ảnh:
- Phim không thuốc cản quang ( NECT): Hình ảnh phim trước cản quang có thể giúp xác định được tính đồng nhất, sự hiện diện các nốt vôi hóa, xuất huyết và ( hoặc ) mỡ trong khối u. Các lát phim mỏng ( 2 – 3 mm) là điều kiện thuận lợi để phát hiện được mô mỡ, giúp xác định được tính chất của khối u. [5]
- Phim có thuốc cản quang ( CECT ) :
- Tăng đậm độ khối u ( ≥ 20 HU so với NECT ):
- Khối u nhỏ dễ bị bỏ sót ở thì vỏ – tủy ( 25s – 70s). [4]
- Đậm độ khối u sẽ kém hơn nhu mô thận ở thì thận đồ ( 80 – 180s ) và ở thì bài tiết ( >180s ). [4]
- Đậm độ không đồng nhất xảy ra khi chảy máu u hoặc hoại tử u. [4]
- Độ nhạy của CT phát hiện được các chồi u trong tĩnh mạch thận 78% và chồi u trong lòng tĩnh mạch chủ khoảng 96%. [2]
- Phát hiện được di căn đến hạch bạch huyết ( ≥ 1cm )
- Xấm lấn các cơ quan lân cận hoặc di căn xa.
- Đánh giá được các nang thận, phát hiện được các nang thận ác tính theo phân độ Bosniak.
- Tăng đậm độ khối u ( ≥ 20 HU so với NECT ):

- Chụp cộng hưởng từ ( MRI: Nuclear Magnetic Resonance Imaging ):
- MRI cho phép phát hiện được các mầm ung thư di căn vào tĩnh mạch thận và tĩnh mạch chủ, đồng thời phát hiện được các di căn cơ quan khác mà không cần sử dụng chất cản quang mạch máu.
- MRI tìm thấy được hình ảnh : [4]
- T1WI :
- Thông thường mật độ u sẽ thể hiện đồng âm ( 60% ) đến giảm âm.
- Tăng tính hiệu đậm độ (SI ) khi xuất huyết trong u.
- T2WI
- ccRCC: tăng SI.
- pRCC: giảm SI.
- Hình ảnh giống như AML nghèo mỡ.
- pRCC có hình ảnh bao giả xung quanh u ( pseudocapsule ).
- T1WI C + FS :
- Đậm độ u lúc nào cũng kém hơn so với nhu mô thận.
- T1WI :
- MRI có lợi đối với những bệnh nhân dị ứng với Iod, suy thận, có thai,..
- Nhược điểm của MRI là giá thành cao hơn so với CT scan nhiều lần, nên vẫn là xét nghiệm được chỉ định khi cần thiết.
- Thủ thuật niệu khoa:
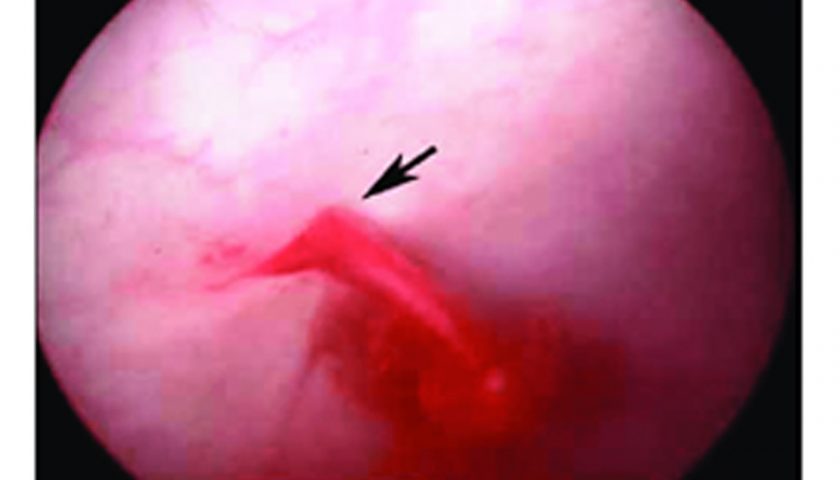
- Nội soi bàng quang chẩn đoán: nội soi bàng quang được chỉ định trong trường hợp tiểu máu do u thận, thấy được máu chảy ra từ miệng niệu quản theo nhịp đập của nhu động, cần thiết trong việc phân biệt tiểu máu do u bàng quang hoặc viêm bàng quang xuất huyết.
- Sinh thiết thận :Sinh thiết chọc dò bằng kim nhỏ được sử dụng khi nghi ngờ về ung thư hoặc khi cần xác định di căn của một ung thư ngoài thận, để có chỉ định thích hợp nên mổ hay không mổ. [1]
- Hình ảnh đồng vị phóng xạ :
- Xác định chức năng của hai thận
- Hiện nay xạ hình còn giá trị trong việc kiểm tra và tìm các tạng hay cơ quan bị di căn như phổi, gan, não, xương….
- Hình ảnh đồng vị phóng xạ :
CHẨN ĐOÁN PHÂN BIỆT
- U đài bể thận.
- U tuyến thượng thận.
- U sau phúc mạc.
- U sợi thần kinh.
- U mỡ.
- U mô cơ, mô sợi.
- Nang thận không điển hình, khi nang có vôi hóa, có vách ngăn.
- AML thận.
TÀI LIỆU THAM KHẢO
| [1] | Nguyễn Bửu Triều và Lê Ngọc Từ, Bệnh học tiết niệu. Ung thư tế bào thận NXB Y học 360 – 373, 2007. |
| [2] | Steven C. Campbell, Brian R. Lane (2020). “Malignant Renal Tumors”, Wein A.: Campbell-Walsh Urology, 12th edition, Saunders Elsevier, vol. 2.. |
| [3] | J. M. M. S. S. C. e. a. Brian I. Rini, AJCC Cancer Staging Manual 8th Edition, 747 – 756, 2018. |
| [4] | A. A. B. M. A. F. M. e. a. (. Mitchell Tublin MD, Dìagnostic Imaging Genitourinary 3th Edition, 202-232. |
| [5] | M. a. I. P. (. 2. ). Alberto Diaz de Leon, Imaging and Screening of Kidney Cancer, Radiol Clin North Am. 2017 Nov; 55(6): 1235–1250.: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5669050/. |
| [6] | L. A. K. B. B. B. Ljungberg, Renal Cell Carcinoma, EAU Guideline , 2019. |
 UNG THƯ HỌC
UNG THƯ HỌC

