ĐẶT VẤN ĐỀ
Các khối u gan được chia làm nhiều loại khác nhau theo tính chất (Lành tính hay ác tính), theo nguồn gốc (Nguyên phát hay thứ phát). Trong các khối u ác tính nguyên phát tại gan, ung thư biểu mô tế bào gan nguyên phát (UTBMTBG) là thể thường gặp nhất, chiếm tỷ lệ xấp xỉ 90%, còn lại là ung thư đường mật trong gan, Sarcoma, Leiomyosarcoma… Bài viết này xin được điểm lại một số bệnh lý ung thư tại gan ngoài UTBMTBG đã được biết đến.
Ung thư di căn gan (Metastases)
Ung thư di căn gan là dạng u ác tính hay gặp nhất tại gan, với tần suất gấp 18 lần các bệnh lý ác tính nguyên phát tại gan như ung thư biểu mô tế bào gan (HCC) [1]. Giá trị của các thăm dò chẩn đoán hình ảnh gan trên những bệnh nhân đã được xác định chẩn đoán ung thư là phát hiện sự hiện diện của tổn thương di căn, đánh giá tính chất ác tính của khối u, và cuối cùng là xác định khả năng cũng như phương án điều trị thích hợp [2].
Đặc điểm hình ảnh di căn gan trên vô cùng đa dạng, tùy theo nguồn gốc của khối u nguyên phát. Hình thái tổn thương tăng sinh mạch dễ dàng nhìn thấy nhất trên phim chụp cắt lớp vi tính thì động mạch, với hình ảnh nốt, khối ngấm thuốc mạnh so với nhu mô gan lân cận. Tình trạng ngấm thuốc ngắn và thường kết thúc trước thì tĩnh mạch cửa. Nguồn gốc u nguyên phát của nhóm di căn tăng sinh mạch bao gồm u thần kinh nội tiết, ung thư tế bào đảo tụy, ung thư hắc tố, ung thư nguyên bào nuôi, u tủy thượng thận, ung thư tuyến giáp và ung thư biểu mô tế bào thận [2].
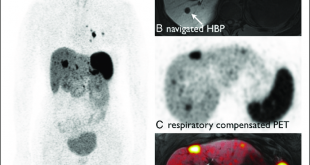
Dạng di căn giảm sinh mạch quan sát rõ nhất trên thì tĩnh mạch cửa của phim chụp cắt lớp vi tính và cộng hưởng từ, với hình ảnh giảm tỷ trọng hay giảm tín hiệu so với vùng nhu mô gan lân cận (Hình 1). Hình thái này hay gặp với ung thư đại trực tràng, ung thư vú, ung thư phổi cũng như ung thư biểu mô tuyến tụy [2].

Cắt lớp vi tính có độ nhạy cao hơn so với cộng hưởng từ với tổn thương canxi hóa, đặc biệt với các tổn thương nhỏ. Đây là hình thái thường gặp với: ung thư cơ trơn đại tràng, dạ dày, tuyến tụy, ung thư tế bào đảo tụy, ung thư mô liên kết, ung thư buồng trứng loại biểu mô tuyến nang thanh dịch thể nhú (papillary serous ovarian cystadenocarcinoma) [3].
Tương tự cắt lớp vi tính, trên công hưởng từ tín hiệu của các khối di căn phụ thuộc vào vị trí nguyên phát, cũng như tình trạng chảy máu hoặc hoại tử. Mặc dù vậy, về cơ bản, hầu hết các u di căn thường giảm tín hiệu trên thì T1 không tiêm thuốc và tăng tín hiệu trên T2 so với nhu mô gan thông thường. Thông thường, các khối di căn thường phân biệt với u máu bởi hầu hết u máu đều tăng tín hiệu trên T2 và có tính chất ngấm thuốc đặc hiệu [4].
Ung thư mô liên kết cơ-mỡ-mạch (Angiomyolipoma)
Đây là nhóm ung thư trung mô hiếm gặp với nhiều thành phần mô bệnh học khác nhau như tổ chức mỡ, cơ trơn và mạch máu [5]. Một số nghiên cứu gần đây lại cho rằng, Angiomyolipoma không phải là khối u có nguồn gốc từ trung mô, mà là một dạng tăng sản có nguồn gốc từ các tế bào biểu mô xung quanh mạch máu (perivascular epithelioid cells). Vì vậy, nó được Tổ chức Y tế Thế giới phân loại là PEComa (“perivascular epithelioid cells” tumor) [6]. Bệnh hay gặp ở phụ nữ trung niên, 50% trường hợp không có triệu chứng lâm sàng. Các triệu chứng thường quan sát được ở nhóm có xuất huyết trong u, thường xảy ra ở nhóm có kích thước khối u trên 5 cm. Bệnh thường có mối liên quan với bệnh xơ cứng củ (tuberous sclerosis) hoặc ung thư mô liên kết xơ-cơ-mỡ tại thận. Rất nhiều bệnh nhân không có biểu hiện triệu chứng gan mật cũng như các Marker ung thư (CEA, CA 19-9) đều âm tính [7].
Do sự hiện diện của nhiều thành phần giải phẫu bệnh khác nhau, Angiomyolipoma thể hiện nhiều hình thái khác nhau trên chẩn đoán hình ảnh. Chỉ 11-25% trường hợp chẩn đoán đúng trước mổ nhờ cắt lớp vi tính và cộng hưởng từ, còn lại đa số trường hợp nhầm lẫn với ung thư biểu mô tuyến [8].
Trên siêu âm, khối u thường có dạng tăng âm và hỗn âm, tương tự với u máu.

Trên cắt lớp vi tính và cộng hưởng từ, với sự hiện diện của một lượng đáng kể tổ chức mỡ trong u, hình ảnh hiện lên với tín hiệu âm tính và giảm tín hiệu trên chuỗi xung out-phase (OOP sequence).

Chẩn đoán phân biệt chính bao gồm các khối u có tổ chức mỡ như u tuyến, ung thư biểu mô tuyến, u mỡ và ung thư mô liên kết dạng mỡ (Liposarcoma) [8].
Như vậy, các yếu tố chính hướng tới chẩn đoán Angiomyolipoma bao gồm:
- Nữ trung niên
- Hình ảnh trên cắt lớp vi tính và cộng hưởng từ tương tự với ung thư biểu mô tuyến, không có triệu chứng gan mật và marker ung thư âm tính.
- Có hiện diện của tổ chức mỡ trong u.
U nang đường mật và Ung thư biểu mô đường mật dạng nang (Cystadenoma and Biliary Cystadenocarcinoma).
U nang đường mật khá hiếm gặp, chiếm nhỏ hơn 5% tất cả trường hợp nang đơn độc hoặc đa nang nguồn gốc từ đường mật [9]. 85% các trường hợp u nang đường mật nằm trong gan, với đường kính từ 1.5 đến 35 cm, xu hướng hay gặp hơn ở gan phải [8]. Hầu hết các trường hợp mắc bệnh là nữ giới trung niên, 5% trường hợp được đánh giá ở giai đoạn tiền ung thư [10]. Triệu chứng lâm sàng thường nghèo nàn, thường do chèn ép bao gồm đau bụng âm ỉ và vàng da [11].
Về đại thể, khối u có dạng nang, bên trong chứa dịch lỏng hoặc nhầy. Thành phần bao gồm máu, dịch mật, hỗn hợp, thậm chí là dịch tinh khiết. Về vi thể, biểu mô lát là biểu mô dạng nhú hoặc polyp, bên cạnh các tế bào mô liên kết hình ovan [8].
Trên cắt lớp vi tính và cộng hưởng từ, u dạng này biểu hiện dưới dạng một nang đơn độc với vỏ nang xơ hóa giới hạn rõ, các nốt xơ cơ, có vách ngăn, canxi hóa và có tỷ trọng dịch [8].


Chẩn đoán phân biệt bao gồm nang nước đơn độc, di căn gan dạng nang và áp-xe [8]
Tóm lại, các yếu tố định hướng chẩn đoán u nang đường mật bao gồm:
- Phụ nữ lứa tuổi trung niên
- Khối nang đơn độc với vách ngăn bên trong, các nốt xơ cơ kèm theo canxi hóa.
Ung thư đường mật trong gan (Inhapetic Cholangiocarcinoma – ICC)
Ung thư đường mật là những khối u ác tính xuất phát từ biểu mô của hệ thống đường mật từ trong gan đến đường mật ngoài gan và đường mật phụ. Theo vị trí giải phẫu ung thư đường mật được chia thành 3 nhóm: Ung thư túi mật, ung thư đường mật và ung thư bóng Vater. Ung thư đường mật lại được chia thành: Ung thư đường mật trong gan, ung thư đường mât vùng rốn gan (U Klatskin) và ung thư phần thấp ống mật chủ. Ung thư đường mật trong gan (intrahepatic cholangiocarcinoma – ICC) hay ung thư đường mật ngoại vi (peripheral cholangicarcinoma – PCC) chiếm 5 -10 % khối ung thư gan nguyên phát và 10% tổng số ung thư đường mật chung [12], [13]. Đây là loại ung thư phổ biến thứ 2 trong số các ung thư nguyên phát tại gan, chỉ xếp sau HCC [14].
Về phân loại giải phẫu bệnh trên đại thể. Hiệp hội ung thư gan Nhật Bản, năm 1997 đã phân 3 loại thương tổn trong ung thư đường mật trong gan dựa trên đặc điểm phát triển của khối u: thể u, thể thâm nhiễm quanh đường mật và thể trong lòng đường mật [14].
Về vi thể, Là những ung thư biểu mô tuyến phát triển từ niêm mạc đường mật. U được cấu tạo bởi một lưới xơ mà trong đó chứa nhiều tuyến có các hình ảnh : ống, nhú hoặc các tế bào tự do (ung thư tế bào vảy, tế bào hạt..). Người ta gọi là các u tuyến khi trong mô có sự hiển diện của các tuyến này (bình thường tuyến chỉ nằm ở lớp niêm mạc), đồng thời các tế bào tuyến có hình ảnh tế bào ung thư (nhân lớn, kiềm tính, mất bào tương, nhiều lớp tế bào…). Khi các đặc trưng mô học của ung thư rõ ràng, số lượng tiêu bản đủ thì việc chẩn đoán mô học thường dễ dàng. Trái lại có thể rất khó xác định giữa ung thư với hình ảnh viêm đường mật hay giữa ung thư với loạn sản, quá sản. Trong viêm xơ đường mật mô liên kết của hệ thống đệm dày, xơ hoá cũng cho hình ảnh tương tự mô ung thư, lúc này những ống tuyến nằm sâu trong thành đường mật vì thế khó phân biệt với ung thư biệt hoá cao.
Bên cạnh các ung thư tuyến biệt hoá (ống, nhú, vách) hay tế bào tự do tuỳ theo vị trí phân bố của tế bào này còn có các dạng khác. Tất cả chúng đều là ung thư biểu mô [15].
- Ung thư biểu mô tuyến (Adenocarcinoma) chiếm hơn 90%.
- Ung thư dạng biểu bì (Epidermoide).
- Ung thư nhầy dạng biểu bì chế nhầy (Mucoepidermoide).
- Ung thư cơ trơn (Leiomyosarcom).
- Ung thư biểu mô tuyến dạng nang (Cystadenocarcinoma).
- Ung thư tế bào hạt (Granular Cell).
- Ung thư tế bào vảy (Squamous).
- Ung thư biểu mô tuyến nhú.
- Thể hỗn hợp giữa UTĐM và ung thư tế bào gan( Hepato Cholangio Carcinoma)
Xâm lấn của các u này thường khu trú tại vùng, di căn ngoài gan rất hiếm, xâm lấn tại chỗ theo mạch máu, ống mật. Đối với xâm lấn vùng nổi trội và xâm lấn hạch (cuống gan). Xâm lấn tạng theo đường kế cận khá hiếm.
Xâm lấn của các u này thường khu trú tại vùng, di căn ngoài gan rất hiếm, xâm lấn tại chỗ theo mạch máu, ống mật. Đối với xâm lấn vùng nổi trội và xâm lấn hạch (cuống gan). Xâm lấn tạng theo đường kế cận khá hiếm.

Siêu âm có thể thấy khối u chiếm tỷ lệ 21 – 47% các trường hợp. Hình ảnh các khối đồng âm với nhu mô gan chiếm 44 – 65%, tăng âm chiếm 33 – 35%, đầu trên có hình cong lõm (hình càng cua), cấu trúc âm này không kèm bóng cản. Thành đường mật có thể bị phá huỷ và khối u phát triển ra xung quanh. Hình ảnh giãn đường mật phía trên là dấu hiệu gián tiếp và thường thấy. Tuy nhiên trong thể thâm nhiễm lan toả đường mật có thể thấy đường mật không giãn. Trường hợp u rốn gan gây dãn đường mật trong gan không gây dãn đường mật chính và không giãn túi mật, các khối u ở phía dưới chỗ đổ vào của ống túi mật sẽ gây giãn túi mật.
Siêu âm có thể đánh giá sự xâm lấn thành đường mật và nhu mô gan của tổn thương ung thư với tỷ lệ 44%. Siêu âm có thể thấy hình ảnh huyết khối TMC hơn là động mạch gan, hiếm hơn nữa là khối hoại tử trong u.

Hình ảnh chụp CLVT của UTĐMTG: thường thấy một khối đồng tỷ trọng hoặc tăng tỷ trọng tương đối đồng nhất trước khi tiêm thuốc cản quang, hiếm gặp giảm tỷ trọng (trong bệnh lý nhiễm ký sinh trùng), khối này thường kèm theo các nốt vệ tinh. Sau khi tiêm thuốc khối u ít ngấm thuốc cản quang, hình ảnh ngấm thuốc trong thì muộn gặp 25 – 55% trường hợp. Đây là dấu hiệu gợi ý chẩn đoán và phân biệt với ung thư tế bào gan. Hiếm gặp có giãn đường mật trong gan. Có thể thấy hình ảnh huyết khối TMC, ĐMG, xâm lấn hạch và hướng dẫn cho chọc sinh thiết u.

Hình ảnh điển hình của khối u trên phim chụp MRI là ở thì T1 khối giảm tín hiệu không đồng nhất, thì T2 tăng tín hiệu không đồng nhất vùng trung tâm giảm tín hiệu, thì T1 tiêm thuốc hình ảnh ngấm thuốc mạnh không đồng nhất vùng trung tâm có vùng giảm tín hiệu


Ung thư tế bào gan dạng xơ dẹt (Fibrolamellar hepatocellular carcinoma – FLC)
Fibrolamellar Carcinoma (FLC) hay còn gọi là ung thư biểu mô tế bào xơ dẹt, chiếm khoảng 1-9% các trường hợp ung thư gan nguyên phát [16]. Loại ung thư này đã được coi là một biến thể mô bệnh học của ung thư biểu mô tế bào gan (HCC), nhưng gần đây nó đã được được công nhận như một thực thể lâm sàng riêng và liên quan đến dịch tễ, nguyên nhân và tiên lượng khác với HCC [17]. Điển hình là những khối u này xảy ra ở những người trẻ (20-40 tuổi) mà không có tiền sử bệnh gan, không liên quan đến các yếu tố xơ gan, nghiện rượu hoặc viêm gan B / C [18].
Về tiên lượng, ung thư biểu mô tế bào xơ dẹt tốt hơn so với ung thư biểu mô tế bào gan nguyên phát: Tỷ lệ sống sau 5 năm của nhiều nghiên cứu lớn của FLC là 67%, trong khi đó với HCC, tỷ lệ này giao động từ 0 đến 25% do từng nghiên cứu [19], [20]. Có thể giải thích do FLC thường xảy ra trong bối cảnh một nhu mô gan bình thường , trong khi HCC xảy ra trong bối cảnh của một xơ gan. Bởi vì xơ gan là yếu tố nguy cơ độc lập đối với tỷ lệ tử vong.
Về triệu chứng lâm sàng, hầu hết không có triệu chứng điển hình nên bệnh nhân thường được phát hiện ở giai đoạn muộn [16]. Các triệu chứng thường gặp nhất bao gồm đau bụng, sờ thấy khối tại vùng gan, chướng bụng và suy kiệt (chiếm 40% số trường hợp) [18], [21]. Một số triệu chứng có thể gặp là đau và sốt khi có tình trạng Abscess hóa, tình trạng nữ hóa ở nam giới do tăng tiết enzyme aromatase, huyết khối tĩnh mạch và vàng da [3].
Về chẩn đoán hình ảnh, FLC có nhiều đặc điểm đặc trưng trên siêu âm, cắt lớp vi tính và cộng hưởng từ.
Trên siêu âm, cấu trúc âm của khối u này tương đối biến đổi, với những vùng tăng cản âm cùng với những vùng giảm cản âm xen kẽ nhau, ngoài ra hình ảnh đặc trưng là nốt trung tâm (central scar), là vùng cản âm nằm ở trung tâm khối u [22].

Trên cắt lớp vi tính thường, FLC hiện lên với hình ảnh giảm tỷ trọng dạng thùy, có thể xuất hiện các vùng giảm âm hơn tương ứng với các nốt trung tâm, vùng hoại tử hoặc chảy máu; trong khi đó hình ảnh canxi hóa gặp trong 15-30% trường hợp [23]. Với cắt lớp vi tính có tiêm thuốc cản quang, ở thì động mạch và tĩnh mạch cửa, FLC hiện lên là một vùng tăng tỷ trọng với những nốt trung tâm giảm tín hiệu. Cuối cùng, ở thì tĩnh mạch hay thì muộn, các nốt trung tâm tăng tín hiệu, trong khi đó phần còn lại, tức là vùng không có hoại tử, với thành phần chủ yếu là mô xơ, sẽ trở nên giảm tỷ trọng [3].

TÀI LIỆU THAM KHẢO
1. Ros PR, Taylor HM (2000). Malignant tumors of the liver. In: Gore RM, Levine MS, eds. Textbook of gastrointestinal radiology, 2nd ed. Philadelphia: WB Saunders:1523–68
2. Jiang K., Al-Diffhala S., and Centeno B.A. (2018). Primary Liver Cancers-Part 1: Histopathology, Differential Diagnoses, and Risk Stratification. Cancer Control J Moffitt Cancer Cent, 25(1), 1073274817744625.
3. Schneider G., Grazioli L., and Saini S. (2006). Imaging of Malignant Focal Liver Lesions. MRI of the Liver: Imaging Techniques, Contrast Enhancement, Differential Diagnosis. Springer Milan, Milano, 187–235.
4. McFarland E.G., Mayo-Smith W.W., Saini S., et al. (1994). Hepatic hemangiomas and malignant tumors: improved differentiation with heavily T2-weighted conventional spin-echo MR imaging. Radiology, 193(1), 43–47.
5. Zhou Y.-M., Li B., Xu F., et al. (2008). Clinical features of hepatic angiomyolipoma. Hepatobiliary Pancreat Dis Int HBPD INT, 7(3), 284–287.
6. Du S., Li Y., Mao Y., et al. (2012). Diagnosis and treatment of hepatic angiomyolipoma. Hepatobiliary Surg Nutr, 1(1), 19–24.
7. Kobayashi Y., Kamimura K., Nomoto M., et al. (2013). Immunohistochemical Character of Hepatic Angiomyolipoma: For Its Management. Case Rep Med, 2013.
8. Mortelé K.J. and Ros P.R. (2001). Cystic focal liver lesions in the adult: differential CT and MR imaging features. Radiogr Rev Publ Radiol Soc N Am Inc, 21(4), 895–910.
9. Billington P.D., Prescott R.J., and Lapsia S. (2012). Diagnosis of a biliary cystadenoma demonstrating communication with the biliary system by MRI using a hepatocyte-specific contrast agent.Br J Radiol, 85(1010), e35-36.
10. Joel J.M., Jeyasingh S.D., and Kalyanaraman S. (2016). Biliary Cystadenoma: A Case Report. J Clin Diagn Res JCDR, 10(2), ED19-ED20.
11. Lewin M., Mourra N., Honigman I., et al. (2006). Assessment of MRI and MRCP in diagnosis of biliary cystadenoma and cystadenocarcinoma. Eur Radiol, 16(2), 407–413.
12. Lim J.H. (2004). Cholangiocarcinoma: recent advances in imaging and intervention. Abdom Imaging, 29(5), 538–539.
13. Fulcher A.S. and Sterling R.K. (2002). Hepatic neoplasms: computed tomography and magnetic resonance features. J Clin Gastroenterol, 34(4), 463–471.
14. Ohtsuka M., Ito H., Kimura F., et al. (2002). Results of surgical treatment for intrahepatic cholangiocarcinoma and clinicopathological factors influencing survival. Br J Surg, 89(12), 1525–1531.
15. Phạm Kim Bình (2015). Hình ảnh giải phẫu bệnh ung thư đường mật được mổ tại bệnh viện Việt-Đức từ 1-2001 đến 30-12-2004. Y Học Việt Nam, 310, 61–67.
16. Pedrassa B.C., da Rocha E.L., Kierszenbaum M.L., et al. (2014). Uncommon hepatic tumors: iconographic essay – Part 1. Radiol Bras, 47(5), 310–316.
17. Corrigan K. and Semelka R.C. (1995). Dynamic contrast-enhanced MR imaging of fibrolamellar hepatocellular carcinoma. Abdom Imaging, 20(2), 122–125.
18. Craig J.R., Peters R.L., Edmondson H.A., et al. (1980). Fibrolamellar carcinoma of the liver: a tumor of adolescents and young adults with distinctive clinico-pathologic features. Cancer, 46(2), 372–379.
19. Pinna A.D., Iwatsuki S., Lee R.G., et al. (1997). Treatment of Fibrolamellar Hepatoma With Subtotal Hepatectomy or Transplantation. Hepatol Baltim Md, 26(4), 877–883.
20. Que F.G. and Nagorney D.M. (1995). Hepatocellular Carcinoma: A Western Perspective. Dig Surg, 12(1), 45–52.
21. Ichikawa T., Federle M.P., Grazioli L., et al. (2000). Fibrolamellar hepatocellular carcinoma: pre- and posttherapy evaluation with CT and MR imaging. Radiology, 217(1), 145–151.
22. McLarney J.K., Rucker P.T., Bender G.N., et al. (1999). Fibrolamellar carcinoma of the liver: radiologic-pathologic correlation. Radiogr Rev Publ Radiol Soc N Am Inc, 19(2), 453–471.
23. Ichikawa T., Federle M.P., Grazioli L., et al. (1999). Fibrolamellar hepatocellular carcinoma: imaging and pathologic findings in 31 recent cases. Radiology, 213(2), 352–361.
 UNG THƯ HỌC
UNG THƯ HỌC